题目内容
13.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如下表所示.他从瓶中倒出100毫升用于配制稀硫酸.求:| 浓硫酸(H2SO44500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封储藏 | |
(2)若将这100毫升浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少?(保留2位小数)
(3)他将一个密度为1.14×103kg/m3,体积为20cm3耐酸小球放在稀硫酸中静止时受到的浮力.(g取10牛/千克)
分析 (1)根据m=ρV,溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(2)根据溶液稀释前后溶质的质量不变,结合题意进行分析解答.
(3)根据F浮=G=mg计算.
解答 解:(1)5mL=50厘米3,m=ρV,这50毫升浓硫酸的质量是1.84克/厘米3×50厘米3=92g,其中含溶质的质量为92g×98%=90.16g;故填:92;90.16g;
(2)溶液稀释前后溶质的质量不变,若将这100毫升浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是$\frac{1.84g/厘{米}^{3}×100厘{米}^{3}×98%}{1.84g/厘{米}^{3}×100厘{米}^{3}+500g}$×100%≈26.4%.故填:26.4%;
(3)稀硫酸溶液的溶质质量分数是26.4%,大于20%,所以硫酸的密度大于1.14g•cm-3,小球在溶液中是漂浮状态,所以小球受到的浮力等于小球的重力,
F浮=G=mg=1.14×103kg/m3×$\frac{20c{m}^{3}}{1000}$×10牛/千克=228牛.故填:228牛.
点评 本题难度不大,掌握溶质质量分数公式、溶液稀释前后溶质的质量不变是正确解答本题的关键.

练习册系列答案
相关题目
1. 等质量的甲、乙两种金属分别与足量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图所示.下列相关判断中,错误的是( )
等质量的甲、乙两种金属分别与足量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图所示.下列相关判断中,错误的是( )
 等质量的甲、乙两种金属分别与足量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图所示.下列相关判断中,错误的是( )
等质量的甲、乙两种金属分别与足量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图所示.下列相关判断中,错误的是( )| A. | 金属活动性乙比甲强 | |
| B. | 若甲是铁,则乙可能是锌;若甲是铝,则乙可能是镁 | |
| C. | 若稀硫酸的质量相等,则甲反应后所得溶液质量比乙大 | |
| D. | 若将相同质量的两种金属都放入足量的硫酸铜溶液中,则甲置换出铜的质量一定比乙多 |
8.测定的下列各数据中,最有可能错误的是( )
| A. | 用10mL量筒量取了7.5mL的水 | |
| B. | 用广范pH试纸测得雨水的pH为5.6 | |
| C. | 用托盘天平称得某固体质量为16.7g | |
| D. | 测得粗盐中氯化钠的质量分数为90.5% |
2.下列实验操作正确的是( )
| A. |  液体加热 | B. |  | C. |  点燃酒精灯 | D. |  |
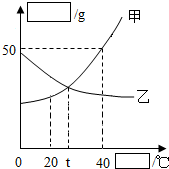 如图是甲、乙两种物质的溶解度曲线图:
如图是甲、乙两种物质的溶解度曲线图:
 家庭厨房就是一个化学小世界,“锅碗瓢盆”、“柴米油盐酱醋茶”中包含着许多化学知识.走进厨房,你会发现煤气罐被方便、价廉的管道天然气代替了,天然气代替煤气罐的优点是(1)环保、方便,便宜;天然气燃烧煮饭时的能量转化为(2)化学能转化为内能生活中自来水的净化经常用活性炭,活性炭在净化水的过程中的作用是(3)过滤不溶性杂质,吸附某些可溶性杂质,除去臭味.也用到漂白粉,漂白粉的制取是氯气和氢氧化钙溶液反应生成氯化钙和次氯酸钙(Ca(ClO)2)和一种常见的氧化物,写出制取漂白粉的化学方程式(4)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,该反应前后氯元素的化合价变化为(5)0价变为-1价和+1价.
家庭厨房就是一个化学小世界,“锅碗瓢盆”、“柴米油盐酱醋茶”中包含着许多化学知识.走进厨房,你会发现煤气罐被方便、价廉的管道天然气代替了,天然气代替煤气罐的优点是(1)环保、方便,便宜;天然气燃烧煮饭时的能量转化为(2)化学能转化为内能生活中自来水的净化经常用活性炭,活性炭在净化水的过程中的作用是(3)过滤不溶性杂质,吸附某些可溶性杂质,除去臭味.也用到漂白粉,漂白粉的制取是氯气和氢氧化钙溶液反应生成氯化钙和次氯酸钙(Ca(ClO)2)和一种常见的氧化物,写出制取漂白粉的化学方程式(4)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,该反应前后氯元素的化合价变化为(5)0价变为-1价和+1价.