题目内容
11.向装有硝酸银、硝酸铜、硝酸铝的混合液中加入一定量的锌粉,充分反应后过滤.(1)若向所得滤渣中滴加稀盐酸,没有气泡产生,则滤渣中一定含有的金属为银.
(2)若向所得滤液中滴加稀盐酸,有白色沉淀产生,则滤液中所含的金属阳离子为Zn2+、Al3+、Ag+、Cu2+.
分析 根据金属活动性强弱关系:铝>锌>氢>铜>银,锌能与硝酸银、硝酸铜依次发生反应而不能与硝酸铝反应,则滤渣中一定无铝,滤液中一定有硝酸锌、硝酸铝.
(1)向所得滤渣中滴加稀盐酸,没有气泡产生,说明锌粉无剩余,一定会有银,可能含有铜,据此分析.
(2)若向所得滤液中滴加稀盐酸,有白色沉淀产生,说明生成氯化银沉淀,说明锌没有把硝酸银置换完,则滤液中一定有硝酸锌、硝酸铝、硝酸银、硝酸铜.
解答 解:
根据金属活动性强弱关系:铝>锌>氢>铜>银,锌能与硝酸银、硝酸铜依次发生反应而不能与硝酸铝反应,则:
(1)向所得滤渣中滴加稀盐酸,没有气泡产生,说明锌粉无剩余,可判断所加入的锌粉一定与硝酸银反应,是否与硝酸铜发生反应因不能确定锌粉的量而无法判断,因此滤液中一定含有没反应的硝酸铝,生成的硝酸锌,可能含有硝酸铜和硝酸银;则滤渣中一定含有的金属为银,可能含有铜.
(2)若向所得滤液中滴加稀盐酸,有白色沉淀产生,说明滤液中含有硝酸银溶液,稀盐酸与硝酸银溶液反应生成氯化银沉淀,说明锌没有把硝酸银置换完,则固体不可能存在铜;由于滤液中含有硝酸银,说明加入的锌粉不足,没能完全置换出溶液中的银离子,所以析出的金属只有银.而此时溶液中含有的溶质有硝酸锌、硝酸铝、硝酸银、硝酸铜.
故答案为:
(1)银;(2)Zn2+、Al3+、Ag+、Cu2+;
点评 本题考查了金属活动性顺序的运用,利用活动性强的金属放入活动性弱的金属的混合盐溶液中,活动性强的金属会先把活动性最弱的金属从其盐溶液中置换出来,然后再置换活动性较弱的金属分析.

练习册系列答案
相关题目
16.分类是一种行之有效、简单易行的科学方法.某同学用下表对所学知识进行分类.下列分类错误的是( )
| 选项 | A | B | C | D |
| 类别 | 单质 | 构成物质微粒 | 有机化合物 | 常见的碱 |
| 物质 | 氧气、臭氧 | 分子、原子、离子 | 甲烷、乙醇 | 烧碱、纯碱 |
| A. | A、 | B. | B | C. | C | D. | D |
3.泡菜具有独特的风味,适合制作泡菜的食盐水浓度是4%.在配制4%的食盐水时,下列操作导致溶液浓度偏小的是( )
| A. | 转移称好的氯化钠固体时,有少量洒在桌上 | |
| B. | 称取氯化钠固体质量偏大 | |
| C. | 转移配好的氯化钠溶液时,有少量液体溅出 | |
| D. | 量取稀释用的水体积偏小 |
20.下列图象能正确反映对应变化关系的是( )
| A. | 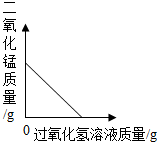 向一定量的MnO2中加入H2O2溶液 向一定量的MnO2中加入H2O2溶液 | |
| B. | 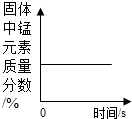 加热一定量的高锰酸钾固体 加热一定量的高锰酸钾固体 | |
| C. | 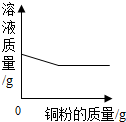 向一定量的硝酸银溶液中加入铜粉 向一定量的硝酸银溶液中加入铜粉 | |
| D. | 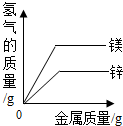 向两份完全相同的盐酸中加入镁和锌 向两份完全相同的盐酸中加入镁和锌 |
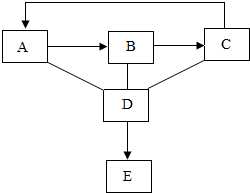 A、B、C、D、E为初中化学常见五种(酸、碱、盐、氧化物、单质)不同类别的物质,它们之间的关系如图所示(“-”表示相连的物质间能发生反应,“→”表示一种物质转化成另一种物质.反应条件、部分反应物和生成物已略去).反应C→A为化合反应,且在反应过程中放出大量热,D是人体胃液中的一种酸,请回答下列问题:
A、B、C、D、E为初中化学常见五种(酸、碱、盐、氧化物、单质)不同类别的物质,它们之间的关系如图所示(“-”表示相连的物质间能发生反应,“→”表示一种物质转化成另一种物质.反应条件、部分反应物和生成物已略去).反应C→A为化合反应,且在反应过程中放出大量热,D是人体胃液中的一种酸,请回答下列问题: