题目内容
3.为探究Al、Fe、Cu三种金属的活动性顺序,有甲、乙、丙三位同学设计了如下方案:(1)甲同学将金属分别放入盛有盐酸的3支试管中,根据铜加入盐酸中无变化以及铝表面产生气泡速率比铁表面产生气泡速率快这两个现象,判断出Al>Fe>Cu.
(2)乙同学只用一支试管,只取一次盐酸也能证明Al>Fe>Cu,他在盐酸中插入金属的顺序是:Fe、Cu、Al;
(3)丙同学认为在乙同学设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论,要补充的实验是把铜放入稀盐酸中;
(4)在CuCl2和AlCl3的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,则滤液中一定含有的溶质是氯化铝、氯化亚铁.
分析 铝比铁活泼,铁比铜活泼,相同条件下,金属和酸反应生成气体的速率越快,说明金属越活泼;
铁能和稀盐酸反应生成氯化亚铁和氢气.
解答 解:(1)铜加入盐酸中无变化,说明铜不能和稀盐酸反应,在金属活动性顺序表中排在氢的后面;
加入稀盐酸中时,铝表面产生气泡速率比铁表面产生气泡速率快,说明铝比铁活泼,并且在金属活动性顺序表中都排在氢的前面,进一步可以判断出Al>Fe>Cu.
故填:铝表面产生气泡速率比铁表面产生气泡速率快.
(2)乙同学只用一支试管,只取一次盐酸也能证明Al>Fe>Cu,他在盐酸中插入金属的顺序是:Fe、Cu、Al,这是因为加入铜时无明显现象,说明铁比铜活泼,再加入铝时,铝表面附着一层固体,说明铝比铁活泼.
故填:Cu、Al.
(3)在乙同学设计的方案中,实验结论是Al>Fe>Cu,如果把铜放入稀盐酸中时,无明显现象,说明金属活动性顺序表中铜排在氢的后面,要得出Al>Fe>H>Cu的结论,需要补充的实验是把铜放入稀盐酸中.
故填:把铜放入稀盐酸中.
(4)在CuCl2和AlCl3的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,说明滤渣中不含有铁,即铁已经完全反应,则滤液中一定含有的溶质是不能反应的氯化铝和反应生成的氯化亚铁.
故填:氯化铝、氯化亚铁.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
11.下列变化中,属于化学变化的是( )
| A. | 雪熔化 | B. | 水结冰 | C. | 冰升华 | D. | 水电解 |
8.下列判断结果正确的是( )
(1)在一溶液中滴入石蕊溶液呈红色,溶液中无H+
(2)HCl、H2S、NH3都是非金属元素与氢的化合物,都属于无氧酸
(3)中性溶液中既没有H+也没有OH-
(4)溶液pH越大H+浓度越大,溶液的酸性越强
(5)10克10%的盐酸和10克10%的氢氧化钠溶液充分混合后,溶液呈中性,pH=7
(6)将pH=5和pH=4的溶液混合后溶液pH=9.
(1)在一溶液中滴入石蕊溶液呈红色,溶液中无H+
(2)HCl、H2S、NH3都是非金属元素与氢的化合物,都属于无氧酸
(3)中性溶液中既没有H+也没有OH-
(4)溶液pH越大H+浓度越大,溶液的酸性越强
(5)10克10%的盐酸和10克10%的氢氧化钠溶液充分混合后,溶液呈中性,pH=7
(6)将pH=5和pH=4的溶液混合后溶液pH=9.
| A. | 只有(1)(3)正确 | B. | 只有(2)(3)正确 | C. | 只有(3)(5)(6)正确 | D. | 都不正确 |
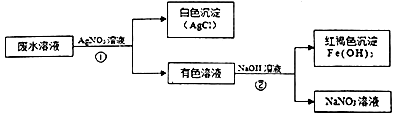
12.某电镀厂在对金属镀件表面除锈、除污过程中,使用盐酸、硫酸、氢氧化钠、碳酸钠等试剂.该厂经处理后排放的废水,仍可能含有 H+、OH-、Na+、Fe3+、Cu2+、CO32-、Cl-、SO42-中的几种离子.某中学学生环保志愿者小组对该废水中部分成分进行检测.实验步骤及现象如下表所示.请你填写下表中每步实验现象所对应的实验结论.

根据以上信息综合分析,请推测该废水中除H2O外,一定含有的物质是NaOH(写化学式,),还不能确定的离子是Cl-、SO42-.

| 实验步骤及现象 | 实验结论(填离子符号) |
| 取废水样品观察,呈无色 | 废水中不含Fe3+、Cu2+ |
| 测所取废水样品的pH,pH=13 | 废水中含较多的OH- |
| 向废水样品中加入过量的稀盐酸,没有气泡产生 | 废水中不含CO32- |
13.溶液与人类的生活息息相关,溶液的配制是日常生活中和化学实验中常见的操作,下表中是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃).请仔细分析列式计算:
(1)取12%的硫酸溶液100毫升可配制成6%的溶液多少克
(2)向200毫升28%的氨水中加入240毫升水,摇匀,溶液的体积是多少毫升?(结果保留一位小数)
| 溶液中溶质的质量分/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/(g/mL) | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/(g/mL) | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(2)向200毫升28%的氨水中加入240毫升水,摇匀,溶液的体积是多少毫升?(结果保留一位小数)