题目内容
2.为了测定石灰石中碳酸钙的质量分数,某兴趣小组的同学称取石灰石样品12.5g2放入烧杯中,然后加入100g稀盐酸,反应后称得烧杯中剩余物的总质量为108.1g(假设杂质不参加反应).求:(1)产生的二氧化碳是4.4g.
(2)石灰石中碳酸钙的质量分数是多少(写出计算过程).
分析 (1)根据该反应中只有二氧化碳是气体,则利用质量守恒定律和反应前后烧杯中物质的总质量之差来计算二氧化碳的质量;
(2)将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量,再计算碳酸钙的质量分数.
解答 解:(1)反应前烧杯中物质的总质量为12.5g+100g=112.5g,反应后烧杯内物质的质量变为108.1g,
由质量守恒可知,二氧化碳的质量为112.5g-108.1g=4.4g;
(2)设碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}$=$\frac{44}{4.4g}$
x=10g
该样品中碳酸钙的质量分数为:$\frac{10g}{12.5g}$×100%=80%.
故答案为:(1)4.4g;
(2)80%.
点评 本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列气体中,能充入灯泡中延长使用寿命的是( )
| A. | H2 | B. | O2 | C. | N2 | D. | CO2 |
14.一定质量的氧化铜及氧化铁分别跟足量的H₂反应.得到的固体质量相等,则氧化铜与氧化铁的质量之比为( )
| A. | 8:7 | B. | 7:8 | C. | 1:2 | D. | 2:1 |
11.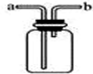 老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
(1)此气体是什么物质?验证它的实验方案如下:
(2)如果用如图所示装置收集我猜想的气体,我认为气体应从a端(填“a”或“b”)导入.
 老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:(1)此气体是什么物质?验证它的实验方案如下:
| 猜 想 | 验证猜想的实验步骤 | 现象及结论 |
| 我认为此气体可能是氧气 | 把带火星的木条伸入集气瓶中 | 木条复燃,证明该气体是氧气 |
| 产生此气体的一个化学方程式是2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | ||
12.要验证Zn.Fe.Cu三种金属的活动性强弱,最好的一组试剂是( )
| A. | Fe、CuSO4溶液、ZnSO4溶液 | B. | Cu、FeCl2溶液、ZnCl2溶液 | ||
| C. | Zn、FeSO4溶液、CuSO4溶液 | D. | Fe、Cu、Zn(NO3)2溶液 |
 某科学兴趣小组成员在查阅资料时了解到:牙膏除主要活性成分外,还有约占牙膏成分50%的CaCO3[或Si02、Al(OH)3、CaHP04]等摩擦剂和保持牙膏湿润的甘油等物质.于是对自己牙膏中的摩擦剂是什么产生了兴趣.
某科学兴趣小组成员在查阅资料时了解到:牙膏除主要活性成分外,还有约占牙膏成分50%的CaCO3[或Si02、Al(OH)3、CaHP04]等摩擦剂和保持牙膏湿润的甘油等物质.于是对自己牙膏中的摩擦剂是什么产生了兴趣.