题目内容
18.如图中的①、②分别是镁元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图,试回答下列问题:
(1)镁元素的原子序数是12,氯元素的相对原子质量是35.45.
(2)A、B、C中化学性质相似的粒子是AB(填序号).
(3)镁元素和氯元素形成的化合物的化学式是MgCl2.
分析 (1)根据图中元素周期表可以获得的信息进行分析解答.
(2)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似.
(3)根据化合物的化学式的写法来分析.
解答 解:(1)由元素周期表中的一格中获取的信息可知,镁元素的原子序数为12;氯的相对原子质量为35.45.故填:12;35.45;
(2)决定元素化学性质的是最外层电子数,原子的最外层电子数相同,具有相似的化学性质,由于A、B的最外层电子数均为7,故具有相似的化学性质.故填:AB;
(3)镁原子最外层有2个电子,易失去2个电子而显+2价,氯原子最外层有7个电子,易得到1个电子而显-1价,故镁元素与氯元素可组成的氯化镁,其化学式为MgCl2.故填:MgCl2.
点评 本题难度不大,掌握灵活运用元素周期表中元素的信息、元素的化学性质与它的原子的最外层电子数目的关系、对元素的概念的理解、常见物质的粒子构成是正确解答本题的关键.

练习册系列答案
相关题目
9.危险发生时,以下应急措施正确的是( )
| A. | 煤气泄漏时,打开电灯检查漏气管道 | |
| B. | 发生火灾时,打开所有门窗通风 | |
| C. | 发现有人触电时,立即用手把触电者拉开 | |
| D. | 地震发生时,在底楼的同学快速跑到空旷的地方 |
6.下列物质中氯元素的化合价最低的是( )
| A. | NaCl | B. | HClO | C. | Cl2 | D. | KClO3 |
13.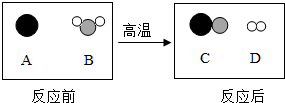 如图为某化学反应的,由此可知该反应的基本反应类型是( )
如图为某化学反应的,由此可知该反应的基本反应类型是( )
 如图为某化学反应的,由此可知该反应的基本反应类型是( )
如图为某化学反应的,由此可知该反应的基本反应类型是( )| A. | 分解反应 | B. | 化和反应 | C. | 置换反应 | D. | 复分解反应 |
10.物质的用途与性质密切相关,下列说法不正确的是化学反应( )
| A. | 食品工业中,小苏打能作发酵粉,是因为小苏打能与面粉反应 | |
| B. | 明矾可用于净水,是因为明矾能与水反应生成具有强吸附性的物质 | |
| C. | 家庭中使用炉具清洁剂能除去油污,是因为清洁剂中有碱性物质,能与油脂发生 | |
| D. | 氢氧化钠固体容易潮解,可用作某些气体的干燥剂 |
7.下列关于溶液的说法正确的是( )
| A. | 溶质可以是固体、液体,也可以是气体 | |
| B. | 同一种溶质在不同溶剂中的溶解能力相同 | |
| C. | 将溶液降低温度,会有晶体析出 | |
| D. | 溶液蒸发溶剂后,溶液的溶质质量分数变大 |
8.下列过程中,发生化学变化的是( )
| A. | 粮食酿酒 | B. | 石头雕像 | C. | 海水晒盐 | D. | 冰雪融化 |