题目内容
16.判断稀盐酸与下表中的四种化合物溶液之间能否发生反应.(1)请仿照示例,在表格②③④处填写“能”或“不能”,并根据复分解反应发生的条件在下表中填写判断依据.
| 氢氧化钠溶液 | 氯化钠溶液 | 碳酸钾溶液 | 硝酸银溶液 | |
| 稀盐酸 | 示例:①能反应 | ②不能反应 | ③能反应 | ④能反应 |
| 判断依据 | 示例:有水生成 | 无气体或沉淀或水生成 | 有气体生成和水 | 有沉淀生成 |
分析 (1)根据复分解反应发生的条件,利用所给的溶解性表,判断下列物质混合能否生成水、或沉淀、或气体而发生复分解反应;
(2)利用氢氧化钠与硫酸反应的化学方程式,根据氢氧化钠的质量求出硫酸的质量.
解答 解:(1)①稀盐酸与氢氧化钠生成水,满足复分解反应的条件,故填:能;有水生成;
②稀盐酸和氯化钠,既无沉淀、也无水、也无气体产生,不能发生复分解反应;故填:不能;无沉淀或无水或无气体生成;
③稀盐酸和碳酸钾反应生成二氧化碳和水气体,符合复分解反应的条件,故填:能;有气体和水生成;
④稀盐酸和硝酸银反应生成氯化银沉淀,符合复分解反应的条件,故填:能;有沉淀生成;
(2)消耗的氢氧化钠溶液中溶质的质量为:80g×20%=16g
设一定量石油产品里含H2SO4的质量为x
2NaOH+H2SO4=Na2SO4+2H2O
80 98
16g x
80:98=16g:x
x=19.6g
故答为:(1)
| 氢氧化钠溶液 | 氯化钠溶液 | 碳酸钾溶液 | 硝酸银溶液 | |
| 稀盐酸 | 示例:①能反应 | ②不能反应 | ③反应 | ④能反应 |
| 判断依据 | 示例:有水生成 | 无气体或沉淀或水生成 | 有气体生成和 | 有沉淀生成 |
点评 本题考查了复分解反应的发生的条件,氢氧化钠的性质以及根据化学方程式的计算,难度不大,但基础知识要扎实.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.公元2世纪,我国古代炼丹家魏伯阳著有的《周易参同契》机世界上现在最早的一部炼丹专著,书中描写道:“金入于猛火,色不夺精光.”“色不夺精光”的解释是黄金没有失去自己的光辉和特性,这句话是指黄金的性质在强热条件( )
| A. | 很稳定 | B. | 易氧化 | C. | 很活泼 | D. | 易还原 |
7.甲、乙、丙、丁四种物质之间转化关系如图所示,则物质甲可能是( )

| A. | SO2 | B. | CuO | C. | Mg | D. | Cu |
4.把4g硫粉放在给定质量的氧气中燃烧,有关实验数据如表所示,请回答
(1)上述实验中,第二次实验恰好完全反应;
(2)上述实验中,第一次实验中硫有剩余;
(3)上述实验中,第三次实验中氧气有剩余,剩余?克;(列化学方程式表达)
(4)在这三次实验中,符合质量守恒定律的是三次都符合.
| 第一次 | 第二次 | 第三次 | |
| O2的质量(g) | 3 | 4 | 6 |
| SO2的质量(g) | 6 | 8 | 8 |
(2)上述实验中,第一次实验中硫有剩余;
(3)上述实验中,第三次实验中氧气有剩余,剩余?克;(列化学方程式表达)
(4)在这三次实验中,符合质量守恒定律的是三次都符合.
11.下面有四种常见的混合物,属于乳浊液的是( )
| A. | 泥水 | B. | 矿泉水 | C. | 生理盐水 | D. | 牛奶 |
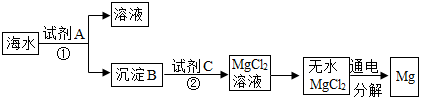
11.海水中溶有少量氯化镁,海边又盛产贝壳(主要成分是CaCO3),某化工厂以它们为主要原料生产镁的大致程序是:
(1)高温煅烧石灰石;(2)用步骤(1)中产生的氧化钙投入到适量的海水中充分反应;
(3)过滤后向滤渣中滴加稀盐酸再进行蒸发;(4)电解熔融氯化镁得到金属镁.
关于该工艺流程,下列说法错误的是( )
(1)高温煅烧石灰石;(2)用步骤(1)中产生的氧化钙投入到适量的海水中充分反应;
(3)过滤后向滤渣中滴加稀盐酸再进行蒸发;(4)电解熔融氯化镁得到金属镁.
关于该工艺流程,下列说法错误的是( )
| A. | 该流程中没有涉及到的基本反应类型是置换反应 | |
| B. | 该流程中涉及到的盐共有3种 | |
| C. | 流程中的起始原料有:石灰石、海水、稀盐酸 | |
| D. | 该流程最终产品有熟石灰、镁、氯气. |
8. 如图所示,将两个燃烧的蜡烛用茶杯罩住,蜡烛全部熄灭后茶杯内壁变黑,下列说法正确的是( )
如图所示,将两个燃烧的蜡烛用茶杯罩住,蜡烛全部熄灭后茶杯内壁变黑,下列说法正确的是( )
 如图所示,将两个燃烧的蜡烛用茶杯罩住,蜡烛全部熄灭后茶杯内壁变黑,下列说法正确的是( )
如图所示,将两个燃烧的蜡烛用茶杯罩住,蜡烛全部熄灭后茶杯内壁变黑,下列说法正确的是( )| A. | 两支蜡烛同时熄灭 | |
| B. | 燃烧产生的二氧化碳使矮小的蜡烛先熄灭 | |
| C. | 蜡烛熄灭说明茶杯内已达真空状态 | |
| D. | 变黑可能是不完全燃烧的产物附着在茶杯内壁造成的 |
9.下列气体中,不能用氢氧化钠固体干燥的是( )
| A. | O2 | B. | SO2 | C. | H2 | D. | CO |