题目内容
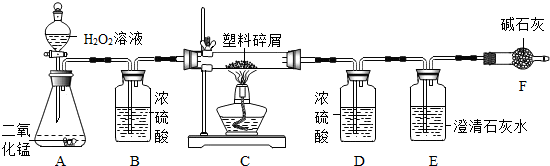
7.今年我国“世界环境日”的主题是向污染宣战,某化工厂排放的废水中含有碳酸钠,提取50g废水样品于集气瓶中,逐滴加入10%的稀硫酸,至恰好完全反应时,收集到 4.4g二氧化碳,请回答问题:(1)判断滴加硫酸至恰好反应的依据是不再产生气泡.
(2)所消耗的稀硫酸质量是多少?
(3)最后所得溶液中溶质的质量分数是多少?(本小题最后结果取整数)
分析 根据质量守恒定律计算出稀硫酸的质量,然后算出溶液的总质量,最后代入数据计算出溶液的溶质质量分数.
解答 解:(1)滴加硫酸至恰好反应的依据是不再产生气泡;
故答案为:不再产生气泡;
(2)设生成4.4克二氧化碳需要稀硫酸的质量是X,生成的硫酸钠的质量为Y.
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
98 142 44
X Y 4.4克
$\frac{98}{X}=\frac{44}{4.4g}$,$\frac{142}{Y}=\frac{44}{4.4g}$,
解得:X=9.8g,Y=14.2g,
所消耗的稀硫酸质量是9.8g÷10%=98g;
(3)最后所得溶液中溶质的质量分数是$\frac{14.2}{98+50-4.4}×100%$≈10%.
点评 培养学生分析题目的能力,掌握化学计算的格式和规范性.

练习册系列答案
相关题目
17.Ⅰ.根据下表信息,用规范的化学用语完成表中空格:
Ⅱ.生活离不开化学,处处留心皆学问,请用下列物质的化学式填空:
①氯化钠 ②乙醇 ③碳酸氢钾 ④硝酸钾
(1)适量饮酒可促进血液循环,这里的“酒”是指C2H5OH.
(2)含作物生长所需营养元素,可作复合肥的是KNO3.
| 化学符号 | 2H | 2N2 | Al3+ | 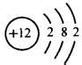 |
| 符号的意义 | 2个氢原子 | 2个氮分子 | 铝离子 | 镁原子的结构示意图 |
①氯化钠 ②乙醇 ③碳酸氢钾 ④硝酸钾
(1)适量饮酒可促进血液循环,这里的“酒”是指C2H5OH.
(2)含作物生长所需营养元素,可作复合肥的是KNO3.
18.将一定质量的含钙元素质量分数为32%的石灰石样品(假设杂质不含钙元素,不溶于水,也不与其他物质反应)高温煅烧一段时间后,剩余固体的质量为20.6g,再向该固体中加入质量分数为7.3%的稀盐酸至恰好完全反应,共用去稀盐酸200g,则煅烧石灰石样品的过程中共生成二氧化碳的质量为( )
| A. | 2.2g | B. | 4.4g | C. | 8.8g | D. | 13.2g |
15.有一种不纯的K2CO3固体,可能含有Na2CO3、MgCO3、NaCl中的一种或几种.取该样品13.8g加入100g稀盐酸,恰好完全反应得到无色溶液,同时产生气体4.4g.下列判断正确的是( )
| A. | 此样品中只有K2CO3 | |
| B. | NaCl不与盐酸反应,样品中一定没有NaCl | |
| C. | 所加稀盐酸中溶质的质量分数为7.3% | |
| D. | Na2CO3和MgCO3都能和盐酸反应生成气体,样品中一定含有Na2CO3和MgCO3 |
16.把质量为100g的铁棒伸入盛有一定量CuSO4溶液烧杯中,充分反应后,取出干燥称量102g,则参加反应的铁的质量为 ( )
| A. | 14g | B. | 8g | C. | 28g | D. | 4g |
17.下列物质属于纯净物的是( )
| A. | 洁净的空气 | B. | 人体呼出的气体 | C. | 自来水 | D. | 液态氮气 |
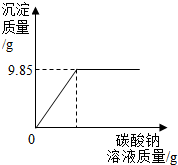 某化工厂技术员小李分析氯化钡和氯化钠组成的产品中氯化钠的质量分数,取16.25g固体样品全部溶于143.6g水中,向所得溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图表示的曲线关系.
某化工厂技术员小李分析氯化钡和氯化钠组成的产品中氯化钠的质量分数,取16.25g固体样品全部溶于143.6g水中,向所得溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图表示的曲线关系.