题目内容
把8g含杂质(杂质不与盐酸反应)的锌粒和足量的稀盐酸反应,待反应停止后,烧杯中物质的质量减少了0.2g.(Zn+2HCl=ZnCl2+H2↑)求:
(1)参加反应的锌的质量;
(2)这种锌粒中含锌的质量分数.
(1)参加反应的锌的质量;
(2)这种锌粒中含锌的质量分数.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:锌和稀盐酸反应生成氯化亚铁和氢气,根据质量守恒定律,烧杯内质量的减少的质量即生成的氢气质量,据此根据反应的化学方程式列式计算出参加反应锌的质量,进而计算出锌的质量分数.
解答:解:质量守恒定律,烧杯内质量的减少的质量即生成的氢气质量,烧杯中物质的质量减少了0.2g,即产生氢气的质量为0.2g.
(1)设参加反应的锌的质量为x
Zn+2HCl=ZnCl2+H2↑
65 2
x 0.2g
=
x=6.5g.
(2)这种锌粒中含锌的质量分数为
×100%=81.25%.
答:(1)参加反应的锌的质量为6.5g;
(2)这种锌粒中含锌的质量分数为81.25%.
(1)设参加反应的锌的质量为x
Zn+2HCl=ZnCl2+H2↑
65 2
x 0.2g
| 65 |
| 2 |
| x |
| 6.5g |
(2)这种锌粒中含锌的质量分数为
| 6.5g |
| 8g |
答:(1)参加反应的锌的质量为6.5g;
(2)这种锌粒中含锌的质量分数为81.25%.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氢气的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
下列没有发生化学变化的是( )
A、 绿色植物光合作用 |
B、 氮气充入食品包装 |
C、 用纯碱蒸制馒头 |
D、 铁锅生锈 |
最近科学家发现,水在-157℃超低温、正常压力或真空条件下仍呈液态,比蜂蜜还粘稠.下列关于这种“高密度液态水”的说法正确的是( )
| A、化学性质与普通水不同 |
| B、分子不再运动 |
| C、该过程发生的是物理变化 |
| D、分子间的间隔比普通水大 |
下列说法正确的是( )
| A、少年儿童不能盲目吃各种营养补品 |
| B、深埋含镉、汞的废旧电池 |
| C、食品添加剂都对健康有害,应禁止使用 |
| D、尽量不要使用铝制餐具,因为铝在人体内积累过多会引起智力下降、记忆力衰退和老年痴呆 |
收集一瓶氢气应采用的方法是( )
| A、向上排气法 | B、排水法 |
| C、排气法 |
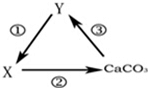 如图表示的是中学化学中常见的物质间的转化关系.请写出写出第②步对应转化关系的化学方程式
如图表示的是中学化学中常见的物质间的转化关系.请写出写出第②步对应转化关系的化学方程式