题目内容
某校兴趣小组用加热氯酸钾和二氧化锰混合物的方法来制取氧气,他们取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并测得相关数据如下表:
试回答:
(1)反应后第 分钟时氯酸钾已全部分解;
(2)完全反应后,生成氧气的质量为 g;
(3)该混合物中二氧化锰的质量是多少?
| 反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| 剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
(1)反应后第
(2)完全反应后,生成氧气的质量为
(3)该混合物中二氧化锰的质量是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)由表中的数据情况可知当反应到2.5秒钟时氯酸钾已经完全反应解答;
(2)欲知完全反应后,生成氧气的质量,须知根据质量守恒定律,反应前后物质的质量总和相等,由此可计算出生成氧气的质量;
(3)欲求原混合物中二氧化锰的质量,需先根据化学方程式,求出氯酸钾的质量.
(2)欲知完全反应后,生成氧气的质量,须知根据质量守恒定律,反应前后物质的质量总和相等,由此可计算出生成氧气的质量;
(3)欲求原混合物中二氧化锰的质量,需先根据化学方程式,求出氯酸钾的质量.
解答:解:
(1)由表中的数据情况可知当反应到2.5秒钟时氯酸钾已经完全反应,
(2)根据质量守恒定律,反应前后物质的质量总和相等,则生成氧气的质量=反应前物质的质量-反应后剩余固体的质量=3.0g-2.04g=0.96g;
(2)解:设原混合物中氯酸钾的质量为x
2KClO3
2KCl+3O2↑
245 96
x 0.96g
=
解得:x=2.45g
该混合物中二氧化锰的质量是3g-2.45g=0.55g
答案:
(1)2.5
(2)0.96
(3)该混合物中二氧化锰的质量是0.55g
(1)由表中的数据情况可知当反应到2.5秒钟时氯酸钾已经完全反应,
(2)根据质量守恒定律,反应前后物质的质量总和相等,则生成氧气的质量=反应前物质的质量-反应后剩余固体的质量=3.0g-2.04g=0.96g;
(2)解:设原混合物中氯酸钾的质量为x
2KClO3
| ||
245 96
x 0.96g
| 245 |
| x |
| 96 |
| 0.96g |
解得:x=2.45g
该混合物中二氧化锰的质量是3g-2.45g=0.55g
答案:
(1)2.5
(2)0.96
(3)该混合物中二氧化锰的质量是0.55g
点评:本题主要考查学生对物质质量守恒定律的认识以及利用化学方程式和质量分数公式进行计算的能力,解题的关键是利用质量守恒定律求出氧气的质量.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
下列是生活中常见的一些变化,其中属于化学变化的是( )
| A、放在衣柜里樟脑球逐渐变小 |
| B、天热吃雪糕时,发现雪糕慢慢熔化 |
| C、洗净的铁锅常会出现锈渍 |
| D、夏天从冰箱取出瓶子外壁迅速附着一层水 |
下列叙述中,正确的是( )
| A、空气是由空气分子构成的 |
| B、氧分子是保持氧气性质的最小粒子 |
| C、氮气和氧气混合后,它们的化学性质都已改变 |
| D、二氧化碳是由碳分子和氧分子构成的 |
下列图示实验操作中,正确的是( )
A、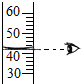 |
B、 |
C、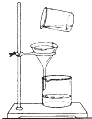 |
D、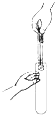 |