题目内容
完成下列实验.
| 实验步骤 | 现象 | 原因 | |
| 向试管中加入5mL 5%的过氧化氢溶液,把带火星的木条伸入试管 |  |
||
| 向上述试管中加入少量二氧化锰,再把带火星的木条伸入试管 |  |
||
考点:实验室制取氧气的反应原理
专题:空气与水
分析:据过氧化氢 常温可分解,但反应比较慢,生成氧气的量较少,二氧化锰可加快过氧化氢的分解速率进行解答.
解答:解:过氧化氢 常温可分解,但反应比较慢,所以向试管中加入5mL 5%的过氧化氢溶液,把带火星的木条伸入试管,可观察到溶液中有气泡产生,但木条不复燃,因为生成氧气的量较少,不足以使带火星的木条复燃;
向上述试管中加入少量二氧化锰,由于二氧化锰可加快过氧化氢的 分解速率,所以溶液中有大量气泡产生,迅速产生较多的氧气,可使带火星的木条复燃;
故答案为:
向上述试管中加入少量二氧化锰,由于二氧化锰可加快过氧化氢的 分解速率,所以溶液中有大量气泡产生,迅速产生较多的氧气,可使带火星的木条复燃;
故答案为:
| 实验步骤 | 现象 | 原因 | |
| 向试管中加入5mL 5%的过氧化氢溶液,把带火星的木条伸入试管 |  |
溶液中有气泡产生,木条不复燃 | 过氧化氢常温下可分解产生氧气,但是反应比较慢 |
| 向上述试管中加入少量二氧化锰,再把带火星的木条伸入试管 |  |
溶液中有大量气泡产生,带火星的木条迅速复燃 | 二氧化锰能加快过氧化氢的分解 |
点评:了解过氧化氢的分解原理,及二氧化锰是过氧化氢反应的催化剂即可顺利解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

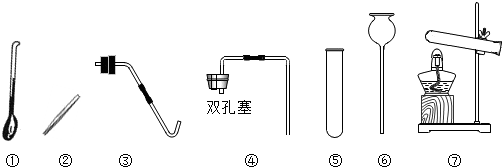
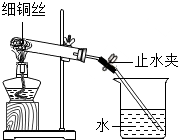 某兴趣小组的同学用如图装置测定空气中氧气的含量.实验过程是:
某兴趣小组的同学用如图装置测定空气中氧气的含量.实验过程是: