题目内容
19.用相同质量的锌和镁分别跟足量的稀硫酸反应,以纵坐标表示生成氢气的质量,横坐标表示反应时间,符合反应实际的图象是( )| A. |  | B. |  | C. |  | D. |  |
分析 在金属活动性顺序中,镁>锌;金属的位置越靠前,与酸反应生成氢气的速度越快,在坐标中表现曲线越陡,相同质量的锌和镁分别和足量的稀硫酸反应,镁产生的氢气量多.
解答 解:根据金属活动性顺序的意义,金属的位置越靠前,与酸反应生成氢气的速度越快,在坐标中表现曲线越陡,相同质量的锌和镁分别和足量的稀硫酸反应,镁产生的氢气量多,观察反应图象,
A、根据生成氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}×金属质量$,则可知相同质量的锌产生的氢气不会比镁多,故A错误;
B、根据金属活动性顺序中镁>锌,锌的反应速度不会比镁快,且产生的氢气质量不会比镁多,故B错误;
C、锌的反应速度不会比镁快,故C错误;
D、根据图象,镁产生的氢气比锌多,速度比锌快,符合题意,故D正确,
故选D.
点评 本题考查了金属活动性顺序的应用,结合生成氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}×金属质量$,可以依据金属活动性顺序的意义进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.固体氢氧化钠需要密封保存是应为氢氧化钠( )
| A. | 易挥发,易吸收空气中的水分 | |
| B. | 易吸收空气中的水分,有腐蚀性 | |
| C. | 有腐蚀性,易与二氧化碳反应 | |
| D. | 易吸收空气中的水分,易与二氧化碳反应 |
10.下列金属中,不能从CuSO4溶液中置换出铜的是( )
| A. | Fe | B. | Ag | C. | Mg | D. | Zn |
7.下列物质的化学式书写正确的是( )
| A. | CaCl | B. | NaCO3 | C. | KCl | D. | CaOH |
4.在化学反应2A+B═2C+D中,若mgA和ngB恰好完全反应生成pgC,则同时生成D的质量是( )
| A. | (m+n-p)g | B. | ($\frac{m}{2}$+n-$\frac{p}{2}$)g | C. | (2m+n-2p)g | D. | (m+n-2p)g |
9.粗盐提纯实验的部分操作如图所示,其中错误的是( )
| A. | 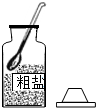 取一定量粗盐 | B. | 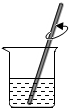 溶解 | C. | 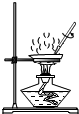 蒸发液体 | D. | 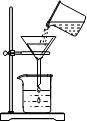 过滤 |