题目内容
18.为了测定KC1化肥中K2CO3的含量,取5g混合物和11.1%的CaCl2溶液做如图实验: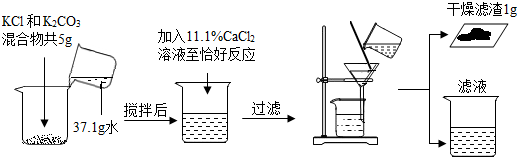
试回答:
(1)写出上述反应的化学方程式K2CO3+CaCl2═CaCO3↓+2KCl;
(2)写出求生成KCl质量(X)的比例式$\frac{100}{1g}$=$\frac{149}{X}$;
(3)该KCl化肥中K2CO3的质量分数为27.6%;
(4)过滤后,最终滤液中溶质的质量分数为10%.
分析 碳酸钾和氯化钙反应生成白色沉淀碳酸钙和氯化钾,根据沉淀碳酸钙的质量可以计算反应生成氯化钾的质量和碳酸钾的质量,进一步可以计算该KCl化肥中K2CO3的质量分数和过滤后,最终滤液中溶质的质量分数.
解答 解:(1)碳酸钾和氯化钙反应的化学方程式为:K2CO3+CaCl2═CaCO3↓+2KCl.
故填:K2CO3+CaCl2═CaCO3↓+2KCl.
(2)设生成氯化钾的质量为X,碳酸钾的质量为Y,氯化钙的质量为Z,
K2CO3+CaCl2═CaCO3↓+2KCl,
138 111 100 149
Y Z 1g X
$\frac{138}{Y}$=$\frac{111}{Z}$=$\frac{100}{1g}$=$\frac{149}{X}$,
X=1.49g,Y=1.38g,Z=1.11g,
故填:$\frac{100}{1g}$=$\frac{149}{X}$.
(3)该KCl化肥中K2CO3的质量分数为:$\frac{1.38g}{5g}$×100%=27.6%.
故填:27.6%.
(4)氯化钙溶液的质量为:1.11g÷11.1%=10g,
最终滤液中溶质的质量分数为:$\frac{5g-1.38g+1.49g}{5g+37.1g+10g-1g}$×100%=10%,
故填:10%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
8.下列化学实验操作中正确的是( )
| A. | 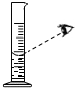 量取液体 | B. | 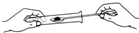 取用固体粉末 | C. | 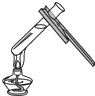 加热液体 | D. | 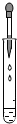 取用液体 |
9.兴趣小组设计了测定空气中氧气 含量的两套实验装置,请结合图示回答问题(装置气密性良好,注射器的摩擦力忽略不计).

(1)装置一和装置二相比,那种装置更环保装置二,写出装置二中发生反应的化学方程式2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;
(2)利用装置二进行实验,记录数据如下.
分析数据,实验测得空气中氧气的体积分数是17.6%;
(3)实验测得的结果出现偏差的原因可能是铜粉的量不足;未待装置完全冷却至室温就读数(答案合理即可).

(1)装置一和装置二相比,那种装置更环保装置二,写出装置二中发生反应的化学方程式2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;
(2)利用装置二进行实验,记录数据如下.
| 盛有铜粉的仪器中空气体积 | 反应前注射器中空气体积 | 反复推拉注射器,当气球恢复原状时,停止推拉并熄灭酒精灯.观察注射器中气体体积 |
| 20mL | 14mL | 8mL |
(3)实验测得的结果出现偏差的原因可能是铜粉的量不足;未待装置完全冷却至室温就读数(答案合理即可).
6.日常生活中,下列做法正确的是( )
| A. | 进入空气不畅通的溶洞,最好用火把进行照明 | |
| B. | 发现厨房煤气泄漏,可立即打开排气扇电源开关 | |
| C. | 用煤炉取暖,可在煤炉上放一壶水以防煤气中毒 | |
| D. | 含糖量较高的粮食,为了防止其霉变可将其放在湿度较大的地方 |
13.除去下列物质中含有的少量杂质,所用试剂和方法都正确的是( )
| 选项 | 物质 | 少量杂质 | 试剂 | 操作方法 |
| A | CO2 | CO | 不用试剂 | 点燃 |
| B | CaCl2溶液 | 稀盐酸 | 加过量的CaCO3粉末 | 搅拌、过滤 |
| C | Fe粉 | CuSO4粉末 | 加足量的水 | 过滤、洗涤晾干 |
| D | 粗盐 | MgCl2 | 过量的NaOH溶液 | 过滤,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
3.下图所示的实验操作正确的是( )
| A. |  稀释浓硫酸 | B. | 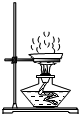 蒸发 | C. |  过滤 | D. | 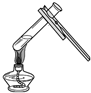 加热液体 |
10.下列实验方法不能达到实验目的是( )
| A. | 用肥皂水鉴别硬水和软水 | |
| B. | 通过观察颜色区别铁丝和铝丝 | |
| C. | 用水区分氯化钠固体和硝酸铵固体 | |
| D. | 通过闻气味区分二氧化硫和二氧化碳 |

 (1)请用化学符号填空:
(1)请用化学符号填空: