题目内容
4.过氧化氢是一种绿色化学试剂,在化学研究及生活中应用广泛.如医疗上常用过氧化氢溶液进行伤口消毒,实验室现有340g过氧化氢溶液和1g二氧化锰,小明让它们在烧杯中反应,完全反应后,烧杯中剩余物质的质量为325g.(1)反应后二氧化锰的质量1g.
(2)生成氧气的质量16g.
(3)过氧化氢溶液中溶质的质量分数是多少?10%.
分析 (1)根据二氧化锰是过氧化氢分解的催化剂,二氧化锰在化学反应前后质量不变进行分析;
(2)根据质量守恒定律计算生成氧气的质量;
(3)根据生成氧气的质量计算参加反应的过氧化氢的质量,然后计算过氧化氢的质量分数.
解答 解:(1)二氧化锰是过氧化氢分解的催化剂,二氧化锰在化学反应前后质量不变进,所以反应后二氧化锰的质量1g;
(2)生成氧气的质量为:340g+1g-325g=16g;
(3)设参加反应的过氧化氢的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 16g
$\frac{68}{x}$=$\frac{32}{16g}$
x=34g
所以过氧化氢溶液中溶质的质量分数是:$\frac{34g}{340g}$×100%=10%.
故答案为:(1)1g;
(2)16g;
(3)10%.
点评 掌握化学方程式的计算格式和规范性,学会使用质量守恒定律是解答本题的关键.

练习册系列答案
相关题目
14.某化学兴趣小组在实验室做了如图所示的A、B两个实验.
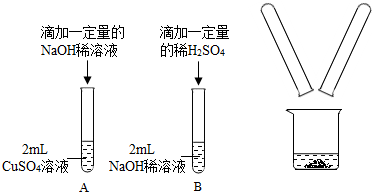
(1)A、B两个实验结束后,小组同学将两支试管中的物质同时倒入一洁净的烧杯中(如图所示),混合后,观察到烧杯中有蓝色沉淀.同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究.
【猜想】小明猜想:滤液中的溶质是Na2SO4、CuSO4:
小光猜想:滤液中的溶质是Na2SO4、NaOH;
小英猜想:滤液中的溶质是Na2SO4、CuSO4、H2SO4;
你的猜想:滤液中的溶质还可能是Na2SO4.
【讨论】你认为小英的猜想一定不合理.
如果滤液为无色,还可排除小明的猜想,理由是硫酸铜溶液是蓝色的.
【实验】若小光的猜想正确,请完成下表的方案.

(1)A、B两个实验结束后,小组同学将两支试管中的物质同时倒入一洁净的烧杯中(如图所示),混合后,观察到烧杯中有蓝色沉淀.同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究.
【猜想】小明猜想:滤液中的溶质是Na2SO4、CuSO4:
小光猜想:滤液中的溶质是Na2SO4、NaOH;
小英猜想:滤液中的溶质是Na2SO4、CuSO4、H2SO4;
你的猜想:滤液中的溶质还可能是Na2SO4.
【讨论】你认为小英的猜想一定不合理.
如果滤液为无色,还可排除小明的猜想,理由是硫酸铜溶液是蓝色的.
【实验】若小光的猜想正确,请完成下表的方案.
| 实验步骤 | 预期的实验现象 | 实验结论 |
| 取少量滤液于试管中,滴入 无色酚酞试液 | 无色酚酞试液变红色 | 小光的猜想正确 |
12.下列气体混合能发生爆炸的是( )
| A. | 煤气和天然气 | B. | 氧气和二氧化碳 | C. | 甲烷和空气 | D. | 氮气和氢气 |

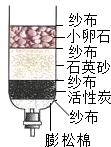 水资源的保护和合理利用已受到人们的普遍关注.请你讨论下列有关问题.
水资源的保护和合理利用已受到人们的普遍关注.请你讨论下列有关问题.