题目内容
(2011?烟台)某环保小组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保小组的同学进行了以下实验.取废水500g,向其中加入溶质质量分数为20%的氢氧化钠溶液.测得沉淀质量与所加入的氢氧化钠溶液的质量关系如下图:根据所得数据计算:
(1)500g该废水中硫酸铜的质量.
(2)该废水中硫酸的溶质质量分数.
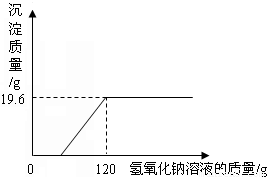
【答案】分析:(1)向含有硫酸和硫酸铜的溶液中加入氢氧化钠溶液,氢氧化钠先与硫酸进行反应,待硫酸完全反应时氢氧化钠继续与硫酸铜发生反应生成氢氧化铜蓝色沉淀;由反应图象中的曲线可得知恰好完全反应时生成沉淀19.6g时消耗氢氧化钠溶液的总质量为120g;根据氢氧化钠与硫酸铜反应的化学方程式,利用生成沉淀的质量可计算出废水中硫酸铜的质量及反应所消耗氢氧化钠的质量;
(2)加入的氢氧化钠总质量与形成沉淀所消耗的质量的差即为中和硫酸时所消耗的氢氧化钠,由此质量可根据反应的化学方程式计算出废水中硫酸的质量,最后利用硫酸质量与500g废水的质量比计算该废水中硫酸的溶质质量分数.
解答:解:(1)设500g废水中CuSO4的质量为x,与CuSO4反应的NaOH溶液的质量为y,
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160 80 98
χ y×20% 19.6g
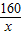 =
=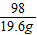 x=32g
x=32g
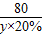 =
=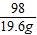 y=80g
y=80g
(2)设500g该废水中H2SO4的质量为z
H2SO4+2NaOH=Na2SO4+2H2O
98 80
z (120g-80g)×20%
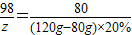
z=9.8g
废水中硫酸的质量分数为 ×100%=1.96%.
×100%=1.96%.
答:(1)500g该废水中CuSO4的质量是32g,
(2)该废水中硫酸的质量分数为1.96%.
点评:对反应的图象中曲线进行分析,该曲线的起点表示硫酸被完全反应、折点表示硫酸铜与氢氧化钠恰好完全反应.
(2)加入的氢氧化钠总质量与形成沉淀所消耗的质量的差即为中和硫酸时所消耗的氢氧化钠,由此质量可根据反应的化学方程式计算出废水中硫酸的质量,最后利用硫酸质量与500g废水的质量比计算该废水中硫酸的溶质质量分数.
解答:解:(1)设500g废水中CuSO4的质量为x,与CuSO4反应的NaOH溶液的质量为y,
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160 80 98
χ y×20% 19.6g
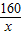 =
=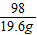 x=32g
x=32g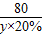 =
=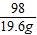 y=80g
y=80g(2)设500g该废水中H2SO4的质量为z
H2SO4+2NaOH=Na2SO4+2H2O
98 80
z (120g-80g)×20%
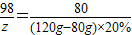
z=9.8g
废水中硫酸的质量分数为
 ×100%=1.96%.
×100%=1.96%.答:(1)500g该废水中CuSO4的质量是32g,
(2)该废水中硫酸的质量分数为1.96%.
点评:对反应的图象中曲线进行分析,该曲线的起点表示硫酸被完全反应、折点表示硫酸铜与氢氧化钠恰好完全反应.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(2011?烟台)某兴趣小组发现一袋腌制松花蛋的泥料,配料表上的成分是氧化钙、纯碱和食盐.他们要探究在腌制松花蛋过程中都有哪些物质对鸭蛋起作用.于是取少量泥料在水中溶解,充分搅拌后过滤,取滤液探究其成分.
【猜想与假设】他们都认为滤液中一定有NaCl和NaOH.生成氢氧化钠的化学方程式为______. 对其他成分他们分别做出了如下猜想:
小亮猜想:还可能有Na2CO3
小强猜想:还可能有Ca(OH)2和Na2CO3
你认为谁的猜想是错误的______,理由是______.你还能做出的猜想是:还可能有______.
【活动与探究】小亮取一定量的滤液于试管中,向其中滴加了几滴稀盐酸,振荡,没有气泡,于是他得出结论:没有Na2CO3.
请你选择CO2以外的物质,设计一个实验方案验证你的猜想.
【反思】小强认为小亮的结论不严密,理由是______.
【猜想与假设】他们都认为滤液中一定有NaCl和NaOH.生成氢氧化钠的化学方程式为______. 对其他成分他们分别做出了如下猜想:
小亮猜想:还可能有Na2CO3
小强猜想:还可能有Ca(OH)2和Na2CO3
你认为谁的猜想是错误的______,理由是______.你还能做出的猜想是:还可能有______.
【活动与探究】小亮取一定量的滤液于试管中,向其中滴加了几滴稀盐酸,振荡,没有气泡,于是他得出结论:没有Na2CO3.
请你选择CO2以外的物质,设计一个实验方案验证你的猜想.
| 实验步骤 | 现象及相应结论 |
| ______ | ______ |