题目内容
9. 多角度认识物质,能帮助我们更全面了解物质世界.以氧气和二氧化碳为例,回答下列问
多角度认识物质,能帮助我们更全面了解物质世界.以氧气和二氧化碳为例,回答下列问(1)认识物质的组成和结构
①从宏观上看,氧气和二氧化碳都含有元素(填“元素”或“分子”下同).
②从微观上看,氧气和二氧化碳都由分子构成.
(2)认识物质的性质
将蘸有酒精的棉芯点燃放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到烧杯中的棉芯自下而上熄灭,如图所示.说明二氧化碳具有的性质有密度比空气的大,不燃烧也不支持燃烧.若使棉芯下半段恢复燃烧,操作方法是将棉芯拿出烧杯.
(3)辩证地认识物质
功过相对论.从“二氧化碳导致温室效应”的事实分析,“过”:使全球气候变暖导致海平面上升等;“功”:为工业生产和植物的光合作用提供丰富的原料.植物光合作用的化学方程式为:6CO2+6H2O $\frac{\underline{\;光、叶绿素\;}}{\;}$ 6O2+X,则X的化学式:C6H12O6;固定和利用二氧化碳的成功范例是:在高温、高压下,以二氧化碳和氨气(NH3)为原料合成尿素[CO(NH2)2],同时有水生成,请写出该反应的化学方程式:CO2+2NH3$\frac{\underline{\;催化剂\;}}{高温}$CO(NH2)2+H2O.
分析 (1)根据二氧化碳和氧气的组成和构成分析回答;
(2)根据实验的现象分析性质,根据燃烧的条件分析若使棉芯下半段恢复燃烧的操作方法;
(3)根据质量守恒定 分析X的化学式,根据题干反应分析反应物、生成物及反应的条件,写出反应的化学方程式.
解答 解:(1)①从宏观上看,氧气和二氧化碳都含有元素;
②从微观上看,氧气和二氧化碳都由分子构成.
(2)将蘸有酒精的棉芯点燃放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到烧杯中的棉芯自下而上熄灭,说明二氧化碳具有的性质有:密度比空气的大,不燃烧也不支持燃烧;由燃烧的条件可知,若使棉芯下半段恢复燃烧,只要有氧气即可,所以操作方法是:将棉芯拿出烧杯;
(3)根据反应的化学方程式6CO2+6H2O $\frac{\underline{\;光、叶绿素\;}}{\;}$ 6O2+X,反应物中碳、氢、氧原子个数分别为6、12、18,反应后的生成物中碳、氢、氧原子个数分别为0、0、12,根据反应前后原子种类、数目不变,则每个X分子由6个碳原子、12个氢原子和6个氧原子构成,则物质X的化学式为C6H12O6;在高温、高压下,以二氧化碳和氨气(NH3)为原料合成尿素[CO(NH2)2],同时有水生成,该反应的化学方程式:CO2+2NH3$\frac{\underline{\;催化剂\;}}{高温}$CO(NH2)2+H2O.
故答为:(1)①元素;②分子.
(2)①密度比空气的大,不燃烧也不支持燃烧;②将棉芯拿出烧杯.
(3)C6H12O6;CO2+2NH3$\frac{\underline{\;催化剂\;}}{高温}$CO(NH2)2+H2O.
点评 本题考查了物质的组成和构成以及常见物质的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.锡是一种银白色熔点低的金属,是大名鼎鼎的“五金”之一,下列说法中错误的是( )


| A. | 锡原子的核内质子数为50 | |
| B. | 锡的化学性质比较活泼,在化学反应中易得电子 | |
| C. | Sn可以表示一个原子 | |
| D. | 锡的相对原子质量为118.7 |
14.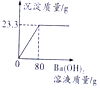 用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:
用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:
试分析并计算:【已知:(NH4)2SO4+Ba(OH)2═BaSO4↓+2NH3↑+2H2O】
(1)硫酸铵中氮元素与氢元素的质量比为7:2.
(2)表格中m的值为1.70.
(3)该氮肥中硫酸铵的质量分数.
 用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:
用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:| 实验次序 | 1 | 2 | 3 |
| 滴入Ba(OH)2溶液的质量/g | 20 | 40 | 60 |
| 生成气体的质量/g | 0.85 | m | 2.55 |
(1)硫酸铵中氮元素与氢元素的质量比为7:2.
(2)表格中m的值为1.70.
(3)该氮肥中硫酸铵的质量分数.
1.下列图象分别与选项中的操作相对应,其中合理的是( )
| A. |  向一定量稀氢氧化钾溶液中滴入水 | |
| B. |  向一定量氯化亚铁溶液中加入过量锌粉 | |
| C. |  向浑浊的石灰水中滴加浓硫酸 | |
| D. |  向少量硫酸和硫酸铁混合溶液中边滴氢氧化钠溶液边振荡 |
19.下列图象能正确反映对应变化的是( )
| A. |  水的电解 | |
| B. |  往氢氧化钠溶液中逐滴加入蒸馏水 | |
| C. |  向盐酸和氯化钙的混合溶液中逐滴加入碳酸钾溶液 | |
| D. |  将足量粉末状金属分别与等质量、等质量分数的稀盐酸反应 |

