题目内容
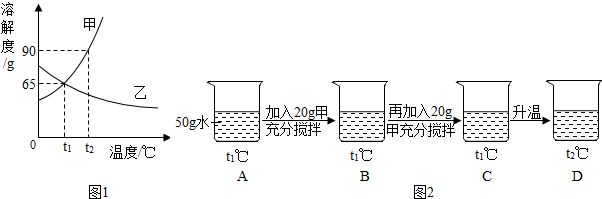
1.如图1是甲、乙两种物质的溶解度曲线,请结合图回答问题:(1)t1℃时,甲、乙两种物质的溶解度相等.
(2)溶解度随温度升高而降低的物质是乙(填“甲”或“乙”).
(3)可使甲物质从其饱和溶液中结晶析出的方法是降低温度,恒温蒸发溶剂(答案合理即可).
(4)t2℃分别将甲、乙两种物质的饱和溶液降温到t1℃,甲溶液的溶质质量分数大于(填“大于”“等于”或“小于”)乙溶液的溶质质量分数.
(5)小明同学用甲物质进行图2实验:
①实验过程中,B、C、D对应的溶液为不饱和溶液的是BD.
②D溶液中溶质的质量分数是44.4%.
分析 (1)根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
(2)根据物质的溶解度曲线可以判断物质的溶解度随着温度的变化而变化的情况;
(3)根据物质的溶解度随着温度的变化而变化的情况可以判断是否析出晶体;
(4)饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
(5)根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液是否饱和.
解答 解:(1)由物质的溶解度曲线可知,t1℃时,甲、乙两种物质的溶解度相等.
故填:t1.
(2)由物质的溶解度曲线可知,溶解度随温度升高而降低的物质是乙.
故填:乙.
(3)由物质的溶解度曲线可知,甲的溶解度随着温度的升高而增大,降低温度,恒温蒸发溶剂可使甲物质从其饱和溶液中结晶析出.
故填:降低温度,恒温蒸发溶剂.
(4)t2℃分别将甲、乙两种物质的饱和溶液降温到t1℃,由于甲在t1℃的溶解度大于乙在t2℃时的溶解度,因此甲溶液的溶质质量分数大于乙溶液的溶质质量分数.
故填:大于.
(5)①实验过程中,t1℃甲的溶解度是65g,B中的50g水溶解20g甲物质形成的是不饱和溶液;
C中的50g水和40g甲物质混合形成的是饱和溶液;
t2℃时,甲的溶解度是90g,D中的50g水和40g甲物质混合形成的是不饱和溶液;
②D溶液中溶质的质量分数为:$\frac{40g}{40g+50g}$×100%=44.4%,
故填:BD;44.4%.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
11.下列化学变化属于置换反应的是( )
| A. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | B. | 3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2 | ||
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | D. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO |
6.食用松花蛋时常感到有涩味,是因为制作过程中用了熟石灰和纯碱等原料.为了减轻涩味,可在食用时加入调味,这种调味品最好是( )
| A. | 食盐 | B. | 食醋 | C. | 香油 | D. | 酱油 |
10.物质的性质往往决定物质的用途,下列关于物质用途的说法中不正确的是( )
| A. | 稀盐酸可用于金属除锈 | B. | 氯化钠可用于制生理盐水 | ||
| C. | 氢氧化钠可用于治疗胃酸过多 | D. | 碳酸钙可用作人体补钙剂 |
11.现有若干克CuO和Cu(OH)2组成的固体混合物,加入100g9.8%g的稀H2SO4充分反应后,所得溶液的pH=7,形成不饱和溶液中铜元素的质量为( )
| A. | 1.2g | B. | 6.4g | C. | 4.8g | D. | 12.8g |
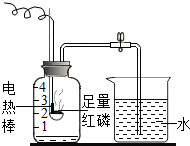 如图是某化学兴趣小组改装的空气中氧气含量的测定实验.按图组装仪器,先检查装置的气密性,再装入过量的红磷,塞上瓶塞,关闭止水夹,通电使红磷燃烧.
如图是某化学兴趣小组改装的空气中氧气含量的测定实验.按图组装仪器,先检查装置的气密性,再装入过量的红磷,塞上瓶塞,关闭止水夹,通电使红磷燃烧.
