题目内容
8.实验室有一瓶长期敞口存放的氢氧化钠固体,同学们推测该氢氧化钠固体已经变质,他们围绕氢氧化钠固体是否全部变质展开探究,并对该固体进行了分离提纯实验.请你根据实验过程及产生的现象作出判断.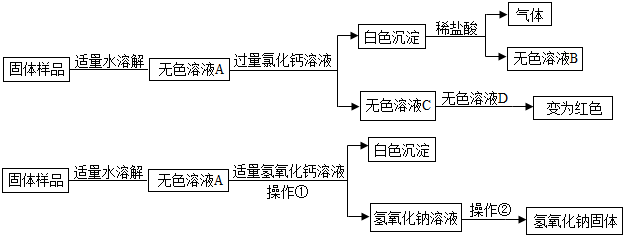
(1)加入的过量氯化钙溶液的目的是将碳酸钠全部除去.无色溶液C中含有的阳离子是Ca2+、Na+.(写粒子符号)
(2)从现象“变为红色”可得出的结论是氢氧化钠部分变质.
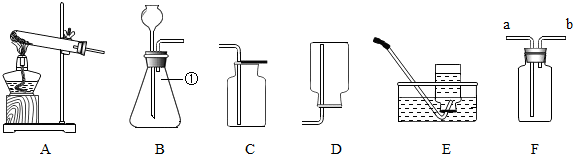
(3)操作①和操作②中都用到的实验仪器有铁架台(带铁圈)、玻璃棒.
(4)无色溶液A中滴加适量氢氧化钙溶液时发生反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
分析 方案一:取样品溶于水得到无色溶液A,加入过量氯化钙溶液,有白色沉淀生成说明氢氧化钠已变质,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,又因为无色溶液C中加入无色溶液D后,溶液变红;说明溶液C中含有碱性物质,说明溶液C中含有氢氧化钠,所以溶液C中含有氢氧化钠、氯化钠及过量的氯化钙;
方案二:取样品溶于水得到无色溶液A,滴加适量氢氧化钙溶液,其中的碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,可以将氢氧化钠中的碳酸钠除去,要将固体和液体分开的操作应为过滤;要从溶液中结晶,可用蒸发操作.
解答 解:方案一:取样品溶于水得到无色溶液A,加入过量氯化钙溶液,有白色沉淀生成说明氢氧化钠已变质,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,又因为无色溶液C中加入无色溶液D后,溶液变红;说明溶液C中含有碱性物质,说明溶液C中含有氢氧化钠,所以溶液C中含有氢氧化钠、氯化钠及过量的氯化钙;
(1)加入的过量氯化钙溶液的目的是将碳酸钠全部除去.溶液C中含有氢氧化钠、氯化钠及过量的氯化钙,含有的阳离子是Ca2+;Na+;
(2)从现象“变为红色”可得出说明溶液C中含有氢氧化钠,说明氢氧化钠部分变质;
方案二:取样品溶于水得到无色溶液A,滴加适量氢氧化钙溶液,其中的碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,可以将氢氧化钠中的碳酸钠除去,要将固体和液体分开的操作应为过滤.
(3)操作①为过滤,操作②为蒸发,都用到的实验仪器有铁架台(带铁圈)、玻璃棒;
(4)无色溶液A中滴加适量氢氧化钙溶液时,碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
故答案为:(1)将碳酸钠全部除去;Ca2+、Na+;
(2)氢氧化钠部分变质;(3)铁架台(带铁圈)、玻璃棒;
(4)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 本考点属于物质的检验、分离和提纯,是中考的重点也是一个难点,本题利用图式设计出相应的实验步骤,分步骤进行分离,同学们只要认真分析,根据条件综合把握,问题就会迎刃而解.本考点经常出现在选择题、填空题和实验题中.

 初中暑期衔接系列答案
初中暑期衔接系列答案| A | 化学与健康 | ①人体缺铁会引起贫血 ②可用甲醛的水溶液浸泡海产品保鲜 |
| B | 化学与环境 | ①使用化石燃料不会对环境产生影响 ②PM2.5是造成雾霾天气的“元凶”之一 |
| C | 化学与安全 | ①图书、档案着火,可用液态二氧化碳灭火 ②在室内放一盆水,可防止煤气中毒 |
| D | 化学与生活 | ①用灼烧闻气味的方法能鉴别棉花和羊毛 ②生活中常用加热煮沸的方法将硬水软化 |
| A. | A | B. | B | C. | C | D. | D |
 和
和 分别表示两种元素的原子,下列有关说法不正确的是( )
分别表示两种元素的原子,下列有关说法不正确的是( )
| A. | 该反应属于化合反应 | B. | 该反应前后元素种类发生了变化 | ||
| C. | 生成物可能是氧化物 | D. | 该反应前后分子种类发生了变化 |
| A. | 农业和园林灌溉,改大水灌溉为喷灌、滴灌 | |
| B. | 改进汽车发动机的燃料方式,使汽油充分燃烧 | |
| C. | 为提高粮食产量,大量使用用各种化肥、农药 | |
| D. | 回收利用废旧金属、废旧书报及废弃燃料 |
| A. | 金属氢是一种新的物质形态 | B. | 金属氢是由两个氢原子构成的 | ||
| C. | 金属氢每个氢原子只有一个电子 | D. | 金属氢可用作火箭的固体燃料 |

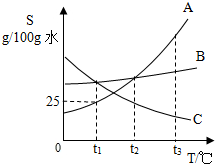 A、B、C三种固体物质溶解度曲线如图所示.
A、B、C三种固体物质溶解度曲线如图所示.