题目内容
17.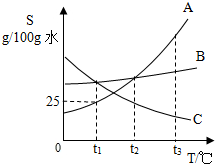 A、B、C三种固体物质溶解度曲线如图所示.
A、B、C三种固体物质溶解度曲线如图所示.①t1℃时,A、B、C三种物质溶解度的大小关系是B=C>A.
②t1℃时,20克A加入到80克水中,完全溶解后,恰好得到饱和溶液.要进一步提高该溶液的溶质质量分数,可进行的操作是升高温度后,增加溶质.
③t3℃时,将等质量A、B、C三种物质分别加水制成相应的饱和溶液,得到溶液
质量最小的是C.(选填“A”、“B”、“C”)
④现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若A中含有少量B,则提纯A的操作步骤是adcb(填字母序号).
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:①通过分析溶解度曲线可知,t1℃时,A、B、C三种物质溶解度的大小关系是B=C>A;
②t1℃时,A物质的溶解度是20g,所以20克A加入到80克水中,完全溶解后,恰好得到饱和溶液,要进一步提高该溶液的溶质质量分数,可进行的操作是升高温度后,增加溶质;
③t3℃时,C物质的溶解度最小,所以将等质量A、B、C三种物质分别加水制成相应的饱和溶液,得到溶液
质量最小的是C;
④现有操作步骤:a、溶解,b、过滤,c、降温结晶,d、加热浓缩;A物质的溶解度受温度影响较大,所以若A中含有少量B,则提纯A的操作步骤是adcb.
故答案为:①B=C>A;
②80,升高温度后,增加溶质;
③C;
④adcb.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
5.俗称与化学式相对应的是( )
| A. | 水银-Ag | B. | 干冰-H2O | C. | 苛性钠-NaOH | D. | 石碱-Na2CO3 |
12.物质间可以直接实现转化的是( )
| A. | Fe→Fe2O3→FeSO4 | B. | HCl→CuCl2→BaCl2 | ||
| C. | NaOH→NaCl→Na2CO3 | D. | CO2→H2CO3→CO |
4.亮亮做家务时接触到下列用品.
①他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁生锈的原因是:Fe与潮湿的空气接触,生锈的化学式是Fe2O3,把还原铁粉在纯氧中燃烧,生成物黑色的Fe3O4(填化学式);
②他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理.
③他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
| 脱氧剂 | 洁厕灵 | 炉灶清洁剂 | |
| 有效成分 | 还原铁粉 | 盐酸 | 氢氧化钠(分解油污,有强烈的腐蚀性) |
②他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理.
③他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
8. 节能减排,保护环境,让“APEC蓝”常在.下列该主题有关的说法或做法错误的是( )
节能减排,保护环境,让“APEC蓝”常在.下列该主题有关的说法或做法错误的是( )
 节能减排,保护环境,让“APEC蓝”常在.下列该主题有关的说法或做法错误的是( )
节能减排,保护环境,让“APEC蓝”常在.下列该主题有关的说法或做法错误的是( )| A. | 燃烧脱硫以减少酸雨的产生 | |
| B. | 积极开发和利用清洁能源 | |
| C. | 加高烟囱排放工业废气 | |
| D. | 温室效应是导致全球气温升高的主要因素之一 |
9.某实验小组的同学向用碳酸钠溶液与饱和石灰水反应来制取氢氧化钠.
(1)该复分解反应能发生的理由是反应能生成碳酸钙沉淀;
(2)有人提出:实验时如果没有注意药品的用量,所得到的氢氧化钠溶液可能不纯.
猜想一:只含NaOH
猜想二:含有NaOH和Na2CO3
猜想三:为了验证猜想一成立,请你根据可选用的试剂,完成实验设计方案并填写以下表格.
可选试剂:NaCl溶液、稀盐酸、Na2CO3溶液
(1)该复分解反应能发生的理由是反应能生成碳酸钙沉淀;
(2)有人提出:实验时如果没有注意药品的用量,所得到的氢氧化钠溶液可能不纯.
猜想一:只含NaOH
猜想二:含有NaOH和Na2CO3
猜想三:为了验证猜想一成立,请你根据可选用的试剂,完成实验设计方案并填写以下表格.
可选试剂:NaCl溶液、稀盐酸、Na2CO3溶液
| 实验步骤 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 取少量所得溶液于试管中,滴入过量的稀盐酸 | 无气泡产生 | 证明原溶液中不含有Na2CO3 |
| 2 | 另取少量所得溶液于试管中,滴入碳酸钠溶液 | 无沉淀生成 | 结合步骤1,证明猜想一成立 |
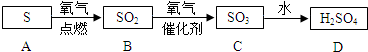 硫元素和人类的生存与发展联系密切,在战国时期,我国的炼丹家们就开始了对硫单质及含硫化合物的研究应用.如图所示是硫及其化合物的转化流程:
硫元素和人类的生存与发展联系密切,在战国时期,我国的炼丹家们就开始了对硫单质及含硫化合物的研究应用.如图所示是硫及其化合物的转化流程: