题目内容
3.金属在日常生活中应用广泛.(1)下列金属制品中,利用金属的导热性的是A.

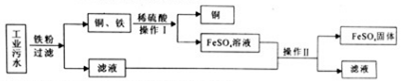
(2)我国湿法冶金早在西汉时期就已开始,其中,“曾青得铁则化为铜”便是佐证,即将铁浸入硫酸铜溶液,该反应的化学方程式为Fe+CuSO4=FeSO4+Cu.
(3)“暖宝宝”中的主要成分是铁粉、氯化钠、活性炭等,其发热原理应用的是铁粉缓慢氧化放热,检验“暖宝宝”是否有效的方法是取少量固体,加入稀盐酸,观察是否有气体产生.
分析 (1)金属具有良好的导电性、导热性和延展性;
(2)铁比铜活泼,能和硫酸铜反应生成硫酸亚铁和铜;
(3)铁能和稀盐酸反应生成氯化亚铁和氢气.
解答 解:(1)下列金属制品中,利用金属的导热性的是铁用作铁锅,铜用作导线是利用了铜的导电性,铂金用作首饰是利用了其延展性.
故选:A.
(2)将铁浸入硫酸铜溶液中时,铁能和硫酸铜反应生成硫酸亚铁和铜,该反应的化学方程式为:Fe+CuSO4=FeSO4+Cu.
故填:Fe+CuSO4=FeSO4+Cu.
(3)检验“暖宝宝”是否有效的方法是:取少量固体,加入稀盐酸,观察是否有气体产生,如果产生气体,说明暖宝宝有效,这是因为没有失效的铁能和稀盐酸反应生成氢气,如果不产生气体,说明暖宝宝已经失效,这是因为失效后的药品不能和稀盐酸反应生成氢气.
故填:取少量固体,加入稀盐酸,观察是否有气体产生.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
8.“类推”是化学学习过程中常用的思维方法.现有以下类推结果,其中正确的是( )
| A. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| B. | 因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 | |
| C. | 金属铝与盐酸反应生产AlCl3和H2,所以金属铁与盐酸反应生产FeCl3和H2 | |
| D. | 点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度 |
9.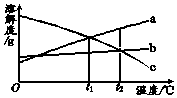 a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
 a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )| A. | 原饱和溶液中,溶质的质量分数a=c>b | |
| B. | 恢复至t1℃时,析出溶质的质量a=c>b | |
| C. | 恢复至t1℃时,三种溶液都是饱和溶液 | |
| D. | 若继续升温至t2℃,三种溶液都是饱和溶液 |
11.现有含氧元素的质量分数为32%的氧化镁、氧化铜组成的混合物40g,与l00g硫酸溶液恰好完全反应,则该硫酸溶液中氢元素的质量分数为( )
| A. | 2% | B. | 4% | C. | 10% | D. | 19.6% |
8.下列描述中只表现物理变化的是( )
| A. | 苛性钠暴露在空气中 | B. | 燃烧着的石蜡也在熔化 | ||
| C. | 往生石灰中加水,把鸡蛋煮熟了 | D. | 活性炭吸附冰箱的异味 |
12.纯碱是我们生活中时常用到的一种材料.晓宇同学想要用实验的方法测得某袋纯碱的纯度,于是他将100g该种纯碱样品放入质量为62g的小烧杯中,随后向其中加入过量的稀盐酸与之反应.整个过程中,他4次称量烧杯和其中物质的总质量,记录在下表中.认为纯碱样品中的其他物质与稀盐酸和水不反应,忽略气体的溶解度,求:
(1)完全反应后,生成二氧化碳的质量为37.4g.
(2)计算该纯碱样品中碳酸钠的纯度.
| 时间t/s | 0 | t1 | t2 | t3 |
| 烧杯总质量/g | 262 | 235.2 | 224.6 | 224.6 |
(2)计算该纯碱样品中碳酸钠的纯度.
13.下列对物质的鉴别方法正确的是( )
| A. | 用水区分氢氧化钠与硝酸铵固体 | |
| B. | 用燃着木条区分二氧化碳与氮气 | |
| C. | 用氧化铜粉末区分稀盐酸与稀硫酸 | |
| D. | 用酚酞试液检验氢氧化钠溶液是否变质 |
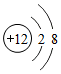 表示的是Mg2+(5)相对分子质量最小的单质是H2
表示的是Mg2+(5)相对分子质量最小的单质是H2