题目内容
8.根据图回答问题.
(1)书写实验仪器名称:①酒精灯 ②分液漏斗
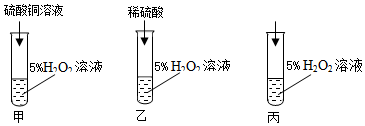
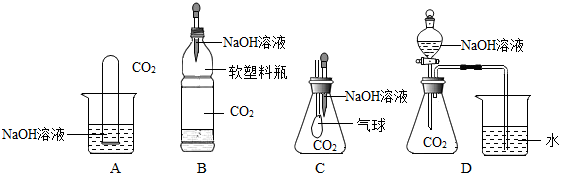
(2)用过氧化氢溶液和二氧化锰来制取氧气时,该反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑可选用的发生装置是B(填序号),其中二氧化锰起催化作用.
(3)用氯酸钾制取氧气时,写出反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,根据该反应原理,可选择图中A(填序号)为发生装置.A装置试管口要略向下倾斜的原因是防止冷凝水倒流引起试管炸裂.
(4)用装置C收集氧气,是因为氧气的性质是氧气的密度比空气大,此方法收集氧气验满的方法是将带火星的木条放于集气瓶口,若木条复燃则满.
(5)用E装置收集氧气,是因为氧气的性质是氧气不易溶于水,此方法判断氧气收集满的方法是集气瓶口有大气泡冒出.
(6)按图F作细铁丝在氧气中燃烧的实验,观察到的现象有铁丝剧烈燃烧,火星四射,放热,生成黑色固体.写出发生反应的化学方程式是3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.实验过程中为了防止集气瓶底部破裂,需要采取的措施是在集气瓶底放一些水或沙子.
(7)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为图1中适合制取乙炔气体的发生装置是B,如果用图2所示装置收集乙炔,气体应从b (填“a”或“b”)端管口通入.
分析 (1)据常用仪器回答;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,据此解答;
(3)加热氯酸钾和二氧化锰的化合物生成氯化钾和氧气,该反应属于固体加热型,故选发生装置A,加热时试管口要略向下倾斜,防止冷凝水倒流引起试管炸裂;
(4)氧气可用向上排空气法收集,因为氧气的密度比空气大,验满氧气的方法是:将带火星的木条放于集气瓶口,观察木条师风复燃进行判断;
(5)氧气可用排水法收集,因为氧气不易溶于水;
(6)据铁丝燃烧的注意事项和 反应原理解答;
(7)据反应物状态和反应条件选择发生装置,据气体密度和溶解性选择收集装置.
解答 解:(1)标号仪器分别是:①是酒精灯;②是分液漏斗;
(2)用过氧化氢溶液和二氧化锰来制取氧气时,发生反应的化学方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;该方法属于固液常温型,故选发生装置B,二氧化锰在反应中起催化作用;
(3)加热氯酸钾和二氧化锰的化合物生成氯化钾和氧气,该反应属于固体加热型,故选发生装置A,加热时试管口要略向下倾斜,防止冷凝水倒流引起试管炸裂;
(4)氧气可用向上排空气法收集,因为氧气的密度比空气大,验满氧气的方法是:将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(5)氧气可用排水法收集,因为氧气不易溶于水;
(6)铁丝在氧气中剧烈燃烧、火星四射,放热,生成黑色固体四氧化三铁,反应方程式是:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;为了防止集气瓶底部破裂,需要在集气瓶底放一些水或沙子;
(7)在常温下用块状电石与水反应制取微溶于水的乙炔,要控制加水速度,以免剧烈反应放热引起发生装置炸裂,则应控制液体的滴加速度,故可选发生装置B,分液漏斗可达到此目的;乙炔密度比水小,所以应从短管进气,长管便于排水;
故答案为:(1)酒精灯;分液漏斗;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;B;催化;
(3)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;A;防止冷凝水倒流引起试管炸裂;
(4)氧气的密度比空气大;将带火星的木条放于集气瓶口,若木条复燃则满;
(5)集气瓶口有大气泡冒出;集气瓶口有大气泡冒出;
(6)火星四射;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;在集气瓶底放一些水或沙子;
(7)B;b.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择,以及制取氧气的注意事项和铁丝燃烧实验等知识,能较好考查学生分析、解决问题的能力.

| A. | 空气中含量最多的气体是N2 | |
| B. | 焚烧垃圾对空气不会造成污染 | |
| C. | 空气中的CO2过多是形成酸雨的主要原因 | |
| D. | 最早发现空气是由N2和O2组成的科学家是中国化学家侯德榜 |
| A. | Al3+-铝元素的化合价为+3 | |
| B. | 3H2O-3个水分子 | |
| C. | 3H-3个氢原子 | |
| D. | SO3-1个三氧化硫分子中含有3个氧原子 |
| 选项 | 事实 | 解释 |
| A | 碘酒是混合物 | 由不同种分子构成 |
| B | 端午时节粽飘香 | 分子在不断运动着 |
| C | 气体受热膨胀 | 温度升高,分子自身体积增大 |
| D | 固体碘受热升华 | 碘分子间的间隔变大 |
| A. | A | B. | B | C. | C | D. | D |
 通过电解水实验可以研究水的组成.电解水的装置如右图3所示,该反应的化学方程式是2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
通过电解水实验可以研究水的组成.电解水的装置如右图3所示,该反应的化学方程式是2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.