题目内容
7.在一个密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质质量如表,下列说法正确的是( )| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量 | 9 | 2 | 22 | 1 |
| 反应后质量 | X | 2 | 6 | 21 |
| A. | X的值是5 | B. | 该反应是分解反应 | ||
| C. | 乙物质一定是催化剂 | D. | 甲和丙是单质,丁是化合物 |
分析 本题可分析先乙、丙、丁三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定甲是反应物还是生成物,进而可以确定反应类型.
解答 解:A、由表中数据分析可知,反应后丁的质量增加了20g,故丁是生成物;乙的质量不变,乙可能作该反应的催化剂,也可能没有参加反应;同理可以确定丙是反应物,参加反应的丙的质量为16g;由质量守恒定律,甲应是反应物,且生成的甲的质量为20g-16g=4g,故X的值是9g-4g=5g,故说法正确.
B、由表中数据分析可知,反应后丁的质量增加了20g,故丁是生成物;乙的质量不变,乙可能作该反应的催化剂,也可能没有参加反应;同理可以确定丙是反应物,参加反应的丙的质量为16g;由质量守恒定律,甲应是反应物,且生成的甲的质量为20g-16g=4g,因此该反应符合“多变一”的特征,属于化合反应,故说法错误.
C、乙的质量不变,乙可能作该反应的催化剂,也可能没有参加反应,故说法错误;
D、根据B选项的分析,该反应属于化合反应,甲和丙是反应物,因此不一定是单质,但丁是生成物,一定是化合物,故说法错误.
故选A.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
17.下列气体能使带火星木条复燃的是( )
| A. | 氧气 | B. | 氮气 | C. | 稀有气体 | D. | 二氧化碳 |
18.今年央视3.15晚会曝光,少数不法厂家向液化石油气中掺入了二甲醚(C2H6O),二甲醚会对液化气罐的配件造成腐蚀,存在安全隐患.下列关于二甲醚的说法正确的是( )
| A. | 属于氧化物 | |
| B. | 它是由两个碳原子、六个氢原子和一个氧原子构成的 | |
| C. | 碳、氢、氧元素的质量比为2:6:1 | |
| D. | 它是由碳、氢、氧三种元素组成的 |
15.下列物质中,属于纯净物的是( )
| A. | 自来水 | B. | 汽水 | C. | 蒸馏水 | D. | 盐水 |
12.市场上有一种自热米饭,其饭盒中有一小包粉末,粉末的主要成分是铁粉、镁粉和氯化钠.小明利用这包粉末,进行了如下的探究实验:
(1)验证并分离铁粉的最简单的物理方法是:把磁铁靠近粉末
(2)若要进一步分离镁粉和氯化钠而得到干燥的镁粉,要进行的操作是:溶解、过滤、洗涤、干燥.在前两步实验操作中都用到的玻璃仪器为烧杯或玻璃棒(填一种)
(3)在(2)所得镁粉中加入一定量的稀硫酸,使固体完全溶解.对所得溶液中含有的溶质,小明作如下猜想:
猜想1:溶质只有硫酸镁.
猜想2:溶质有硫酸镁和H2SO4(填化学式)
设计实验:小明选用一种金属单质进行实验
写出此实验探究步骤中发生反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑.
(1)验证并分离铁粉的最简单的物理方法是:把磁铁靠近粉末
(2)若要进一步分离镁粉和氯化钠而得到干燥的镁粉,要进行的操作是:溶解、过滤、洗涤、干燥.在前两步实验操作中都用到的玻璃仪器为烧杯或玻璃棒(填一种)
(3)在(2)所得镁粉中加入一定量的稀硫酸,使固体完全溶解.对所得溶液中含有的溶质,小明作如下猜想:
猜想1:溶质只有硫酸镁.
猜想2:溶质有硫酸镁和H2SO4(填化学式)
设计实验:小明选用一种金属单质进行实验
| 实验步骤 | 实验现象 | 结论 |
| 取所得溶液少量于试管中加入 锌粒 | 猜想1成立 | |
16.化学变化的实质是( )
| A. | 分子运动速度加快 | |
| B. | 分子分裂成原子,原子重新组合成其他物质的分子 | |
| C. | 分子间隔变小 | |
| D. | 一种分子运动到另一个物质的分子之间去 |
 如图是验证分子性质的装置.U型管左侧管内固定一小试管,右侧管内挂有滴有酚酞溶液的滤纸条,胶头滴管中有浓氨水.
如图是验证分子性质的装置.U型管左侧管内固定一小试管,右侧管内挂有滴有酚酞溶液的滤纸条,胶头滴管中有浓氨水.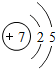 氮原子最外层电子数为5.
氮原子最外层电子数为5.