题目内容
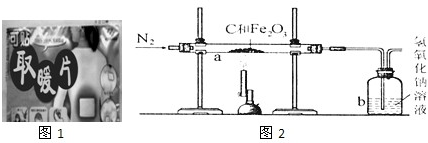
铁是生活中常用的金属.是某“取暖片”外包装的图片(如图1).该“取暖片”中发热剂主要成分有铁粉、氯化钠、水、活性炭等,其发热是利用铁生锈时会放热的原理.
(1)①发热剂需接触到空气才会发热,原因是铁要与 和 共同作用才会生锈.
②推测发热剂成分中氯化钠的作用是 .
③举例生活中防止金属铁生锈的两种方法: 、 .
(2)化学兴趣小组的甲、乙、丙、丁四位同学对“取暖片”的成分产生了兴趣.
Ⅰ.甲同学预测定“取暖片”中铁粉的含量.取5.7g“取暖片”样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量10.0g)中.在化学反应过程中对烧杯进行了五次称量,数据记录如下表:
①表格中m的值为 克;反应中共产生氢气 克;
②“取暖片”样品铁粉的质量分数 (精确到0.1%)
③乙同学提出质疑,他认为甲同学的实验测定方案不合理,会导致Fe%结果偏大,试分析可能的原因:
Ⅱ.丙同学预测定一包已变质“取暖片”中Fe2O3的质量分数.取10g已变质“取暖片”样品与过量的木炭粉混合,如图2所示装置完成实验.(木炭粉有还原性,NaOH溶液用来吸收反应生成的CO2,杂质不参加反应)
①实验中持续通入干燥的氮气,加热前缓缓通入一段时间的作用是
②直玻璃管中发生的反应方程式
③充分反应后,丙同学测定NaOH溶液的质量增加了3.3g,通过计算帮助丙同学求出已变质“取暖片”样品中Fe2O3的质量分数.
④丁同学提出质疑,他认为丙同学的测定方案不合理,会导致Fe2O3%的结果偏小,说一说他的理由: (1条即可)

(1)①发热剂需接触到空气才会发热,原因是铁要与
②推测发热剂成分中氯化钠的作用是
③举例生活中防止金属铁生锈的两种方法:
(2)化学兴趣小组的甲、乙、丙、丁四位同学对“取暖片”的成分产生了兴趣.
Ⅰ.甲同学预测定“取暖片”中铁粉的含量.取5.7g“取暖片”样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量10.0g)中.在化学反应过程中对烧杯进行了五次称量,数据记录如下表:
| 反应时间 | t0 | t1 | t2 | t3 | t4 |
| 烧杯和药品质量/g | 25.7 | 25.6 | 25.5 | 25.5 | m |
②“取暖片”样品铁粉的质量分数
③乙同学提出质疑,他认为甲同学的实验测定方案不合理,会导致Fe%结果偏大,试分析可能的原因:
Ⅱ.丙同学预测定一包已变质“取暖片”中Fe2O3的质量分数.取10g已变质“取暖片”样品与过量的木炭粉混合,如图2所示装置完成实验.(木炭粉有还原性,NaOH溶液用来吸收反应生成的CO2,杂质不参加反应)
①实验中持续通入干燥的氮气,加热前缓缓通入一段时间的作用是
②直玻璃管中发生的反应方程式
③充分反应后,丙同学测定NaOH溶液的质量增加了3.3g,通过计算帮助丙同学求出已变质“取暖片”样品中Fe2O3的质量分数.
④丁同学提出质疑,他认为丙同学的测定方案不合理,会导致Fe2O3%的结果偏小,说一说他的理由:
考点:金属锈蚀的条件及其防护,实验探究物质的组成成分以及含量,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:金属与金属材料
分析:(1)铁与水和氧气充分接触时容易生锈,盐溶液能够促进铁生锈;
(2)铁与盐酸能反应生成氢气;根据氢气的质量求算铁的质量;根据一氧化碳于氧化铁的反应进行分析判断即可.
(2)铁与盐酸能反应生成氢气;根据氢气的质量求算铁的质量;根据一氧化碳于氧化铁的反应进行分析判断即可.
解答:解:(1)①铁要与氧气和水共同作用才会生锈,故填:氧气,水;
②盐存在时,会使铁生锈的速度加快,故填:加快铁的生锈速度;
③防锈就是破坏铁生锈的条件,可以刷漆或者涂油,故填:刷漆,涂油;
(2)Ⅰ①t1和t2时烧杯中的质量相同,故反应进行完全,质量不再改变,m=25.5,生成氢气的质量为5.7g+10.0g+10.0g-25.5g=0.2g,故填:25.5,0.2;
②设铁的质量为x
Fe+2HCl═FeCl2+H2↑
56 2
x 0.2g
=
x=5.6g
铁的质量分数为:
×100%≈98.2%;
③产生的氢气从溶液中逸出,会带出水蒸气,导致测得氢气的质量偏大,从而铁的质量分数偏大,故填:产生的氢气从溶液中逸出,会带出水蒸气,导致测得氢气的质量偏大;
Ⅱ①实验中持续通入干燥的氮气,加热前缓缓通入一段时间的作用是排尽装置内的空气,防止加热时产生爆炸,故填:排尽装置内的空气;
②碳和氧化铁在高温的条件下反应生成铁和二氧化碳,故填:3C+2Fe2O3
4Fe+3CO2;
③NaOH溶液的质量增加了3.3g,说明生成二氧化碳的质量是3.3g,设氧化铁的质量为x
3C+2Fe2O3
4Fe+3CO2
320 132
x 3.3g
=
x=8g
已变质“取暖片”样品中Fe2O3的质量分数为:
×100%=80%;
④木炭过量,则在高温的条件下木炭会与生成的二氧化碳反应生成一氧化碳,导致二氧化碳的质量偏小,从而计算的氧化铁的质量分数偏小,故填:在高温的条件下木炭会与生成的二氧化碳反应生成一氧化碳,导致二氧化碳的质量偏小.
②盐存在时,会使铁生锈的速度加快,故填:加快铁的生锈速度;
③防锈就是破坏铁生锈的条件,可以刷漆或者涂油,故填:刷漆,涂油;
(2)Ⅰ①t1和t2时烧杯中的质量相同,故反应进行完全,质量不再改变,m=25.5,生成氢气的质量为5.7g+10.0g+10.0g-25.5g=0.2g,故填:25.5,0.2;
②设铁的质量为x
Fe+2HCl═FeCl2+H2↑
56 2
x 0.2g
| 56 |
| x |
| 2 |
| 0.2g |
铁的质量分数为:
| 5.6g |
| 5.7g |
③产生的氢气从溶液中逸出,会带出水蒸气,导致测得氢气的质量偏大,从而铁的质量分数偏大,故填:产生的氢气从溶液中逸出,会带出水蒸气,导致测得氢气的质量偏大;
Ⅱ①实验中持续通入干燥的氮气,加热前缓缓通入一段时间的作用是排尽装置内的空气,防止加热时产生爆炸,故填:排尽装置内的空气;
②碳和氧化铁在高温的条件下反应生成铁和二氧化碳,故填:3C+2Fe2O3
| ||
③NaOH溶液的质量增加了3.3g,说明生成二氧化碳的质量是3.3g,设氧化铁的质量为x
3C+2Fe2O3
| ||
320 132
x 3.3g
| 320 |
| x |
| 132 |
| 3.3g |
已变质“取暖片”样品中Fe2O3的质量分数为:
| 8g |
| 10g |
④木炭过量,则在高温的条件下木炭会与生成的二氧化碳反应生成一氧化碳,导致二氧化碳的质量偏小,从而计算的氧化铁的质量分数偏小,故填:在高温的条件下木炭会与生成的二氧化碳反应生成一氧化碳,导致二氧化碳的质量偏小.
点评:本题考查了金属的有关性质以及根据化学方程式的计算,完成此题,可以依据已有的知识结合题干题干的信息进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在下列几组物质中,含有相同原子团的是( )
| A、KMnO4、K2MnO4 |
| B、NaOH、H2O |
| C、KNO3、KClO3 |
| D、NaOH、Ca(OH)2 |

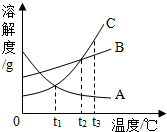 如图中A、B、C分别表示三种物质的溶解度曲线.
如图中A、B、C分别表示三种物质的溶解度曲线. 能源与环境已成为人们关注的热点.
能源与环境已成为人们关注的热点.