题目内容
实验室用过氧化氢制取氧气,如果要制得氧气的质量为16克,那么需要过氧化氢的质量是多少,同时生成的水的质量又是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据生成氧气的质量结合反应的化学方程式可以计算出消耗的过氧化氢的质量以及生成水的质量即可.
解答:解:设需要过氧化氢的质量x,生成水的质量为y.
2H2O2
2H2O+O2↑
68 36 32
x y 16g
=
=
x=34g y=18g
答:理论上消耗过氧化氢的质量是34g;同时生成水的质量为18g.
2H2O2
| ||
68 36 32
x y 16g
| 68 |
| x |
| 36 |
| y |
| 32 |
| 16g |
x=34g y=18g
答:理论上消耗过氧化氢的质量是34g;同时生成水的质量为18g.
点评:在利用反应的化学方程式进行计算时,首先要正确书写化学方程式,此外还要注意:解、设、答要完整,已知物质与未知物质的质量关系及比例式要正确写出,计算过程中要带单位.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
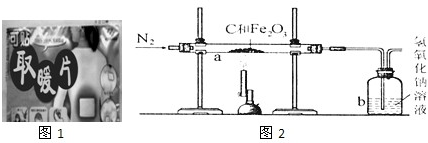
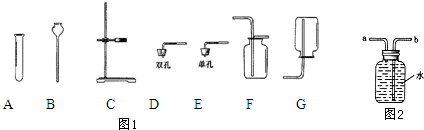
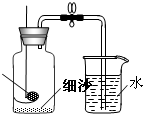 在”空气中氧气含量的测定”实验探究中,小明进行如下实验:将红磷盛放在燃烧匙中,点燃后立即插入集气瓶内并塞上瓶塞.
在”空气中氧气含量的测定”实验探究中,小明进行如下实验:将红磷盛放在燃烧匙中,点燃后立即插入集气瓶内并塞上瓶塞.