题目内容
 为了研究炼铁原理,我市某校九年级综合实践活动小组按如图所示,用一氧化碳与氧化铁反应进行实验,现请你一起参与.
为了研究炼铁原理,我市某校九年级综合实践活动小组按如图所示,用一氧化碳与氧化铁反应进行实验,现请你一起参与.(1)该实验开始时,要先通一会儿一氧化碳再加热,其目的是
(2)如图所示试管中发生反应的化学方程式是
反应停止后,同学们对冷却后玻璃管内固体物质的组成成分产生了兴趣,大家纷纷提出自己的猜想.请将你的猜想写出:
猜想一:
猜想二:
考点:一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)做一氧化碳还原氧化铁实验时,对于一氧化碳是“早出晚归”,酒精灯是“迟到早退”;
(2)一氧化碳与氧化铁反应产物为二氧化碳和铁,二氧化碳能使澄清石灰水变浑浊;尾气中含有一氧化碳,有毒会污染空气;氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,氧化铁是红色的,铁粉是黑色的;为了防止高温生成的铁被重新氧化,所以要先停止加热,再停止通入一氧化碳;如果氧化铁被完全还原,则玻璃管中得到的黑色物质为铁,若氧化铁未被完全还原,则玻璃管内固体物质为铁和氧化铁的混合物,据此分析解答.
(2)一氧化碳与氧化铁反应产物为二氧化碳和铁,二氧化碳能使澄清石灰水变浑浊;尾气中含有一氧化碳,有毒会污染空气;氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,氧化铁是红色的,铁粉是黑色的;为了防止高温生成的铁被重新氧化,所以要先停止加热,再停止通入一氧化碳;如果氧化铁被完全还原,则玻璃管中得到的黑色物质为铁,若氧化铁未被完全还原,则玻璃管内固体物质为铁和氧化铁的混合物,据此分析解答.
解答:解:(1)实验开始时,要先通一会儿一氧化碳再加热,其目的是排净玻璃管内空气,防止一氧化碳与空气在高温下混合发生爆炸;
(2)试管中发生反应是二氧化碳和澄清石灰水反应,产物为碳酸钙和水,化学方程式是:CO2+Ca(OH)2═CaCO3↓+H2O;导管口点燃酒精灯的目的是使未参加反应的一氧化碳燃烧掉,防止排到空气中污染空气;氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,氧化铁是红色的,铁粉是黑色的;实验完毕后,要先停止加热,等到装置冷却至室温,再停止通入一氧化碳,以免高温生成的铁被重新氧化.
如果氧化铁被完全还原,则玻璃管中得到的黑色物质为铁,若氧化铁未被完全还原,则玻璃管内固体物质为铁和氧化铁的混合物.
故答案为:(1)排净试管内空气,防止一氧化碳与空气在高温下混合发生爆炸;(2)CO2+Ca(OH)2═CaCO3↓+H2O;尾气处理;红色粉末变黑色;停止加热;停止通一氧化碳;防止高温生成的铁被重新氧化;固体物质可能是Fe;固体物质可能是Fe和Fe2O3的混合物.
(2)试管中发生反应是二氧化碳和澄清石灰水反应,产物为碳酸钙和水,化学方程式是:CO2+Ca(OH)2═CaCO3↓+H2O;导管口点燃酒精灯的目的是使未参加反应的一氧化碳燃烧掉,防止排到空气中污染空气;氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,氧化铁是红色的,铁粉是黑色的;实验完毕后,要先停止加热,等到装置冷却至室温,再停止通入一氧化碳,以免高温生成的铁被重新氧化.
如果氧化铁被完全还原,则玻璃管中得到的黑色物质为铁,若氧化铁未被完全还原,则玻璃管内固体物质为铁和氧化铁的混合物.
故答案为:(1)排净试管内空气,防止一氧化碳与空气在高温下混合发生爆炸;(2)CO2+Ca(OH)2═CaCO3↓+H2O;尾气处理;红色粉末变黑色;停止加热;停止通一氧化碳;防止高温生成的铁被重新氧化;固体物质可能是Fe;固体物质可能是Fe和Fe2O3的混合物.
点评:本题考查一氧化碳还原氧化铁实验,了解实验步骤和注意事项、反应原理,即可顺利解答,猜想要有相关的事实依据,不能凭空猜想.

练习册系列答案
相关题目
物质的结构决定物质的性质,下列关于物质结构与性质的说法不正确的是( )
| A、一氧化碳具有还原性,二氧化碳没有,是由于分子构成不同 |
| B、铁在空气中易生锈,铝在空气中抗腐蚀能力很强,是由于金属活动性顺序不同 |
| C、金刚石是无色透明的晶体,石墨是黑色的有金属光泽的细鳞片状固体,是由于碳原子的排列方式不同 |
| D、铁块在空气中不能燃烧,纳米级铁粉在空气中可以自燃,是由于铁与空气的接触面积不同 |
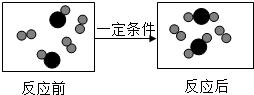 一定条件下,物质A(
一定条件下,物质A( )与B(
)与B( )反应生成C(
)反应生成C( ),下图是其反应前后分子及其数目变化的微观示意图.
),下图是其反应前后分子及其数目变化的微观示意图.

