题目内容
18.鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小王和小明同学进行了如下实验:他俩将蛋壳洗净、干燥并捣碎放在烧杯里,然后往烧杯中加入足量盐酸.实验过程和测定的相关实验数据如
图所示:

(1)小王根据“蛋壳残渣4.3g”,求得蛋壳中碳酸钙质量分数为57%.
小明根据“反应过程中减少的质量”也求得了蛋壳中碳酸钙的质量分数,请你写出小明的计算过程和结果.
(H:1 C:12 O:16 Cl:35.5 Ca:40)
(2)小王和小明根据不同的数据求得蛋壳中碳酸钙的质量分数有明显差别,请你分析其中可能的原因.
分析 利用质量守恒定律,由反应前后各物质质量总和的差值,计算出反应放出二氧化碳的质量;由二氧化碳的质量,根据反应的化学方程式,计算出鸡蛋壳中所含量碳酸钙的质量,即可求得该鸡蛋壳中碳酸钙的质量分数.
解答 解:
(1)蛋壳中碳酸钙的质量为 10g-4.3g=5.7g
鸡蛋壳中碳酸钙的质量分数为:$\frac{5.7g}{10g}$×100%=57%
根据质量守恒定律,产生二氧化碳的质量=10g+100g-106.7g=3.3g,所以丁同学的计算过程为:
设鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{x}$=$\frac{44}{3.3g}$
x=7.5g
该鸡蛋壳中碳酸钙的质量分数=$\frac{7.5g}{10g}$×100%=75%
(2)丙同学计算所用的蛋壳残渣可能未干燥,实际蛋壳残渣质量小于4.3克或丁同学计算所用的数据“3.3g”中包含了反应过程中盐酸挥发了的氯化氢气体的质量,即实际生成的二氧化碳气体质量小于3.3g
故答案为:
(1)57%;
设鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{x}$=$\frac{44}{3.3g}$
x=7.5g
该鸡蛋壳中碳酸钙的质量分数=$\frac{7.5g}{10g}$×100%=75%
(2)丙同学计算所用的蛋壳残渣可能未干燥,实际蛋壳残渣质量小于4.3g
点评 在进行表格计算时,首先学会分析表格的数据,通常要用到质量守恒定律,然后由数据得到化学方程式中的一部分数据,然后利用化学方程式进行计算,考查学生分析、解决问题的能力.

| A. | H+、Na+、OH${\;}^{_}$、SO${\;}_{4}^{2-}$ | B. | K+、Na+、Cl-、CO${\;}_{3}^{2-}$ | ||
| C. | Cl-、CO${\;}_{3}^{2-}$、Ca2+、Na+ | D. | NH${\;}_{4}^{+}$、Na、OH-、NO${\;}_{3}^{-}$ |
 化学兴趣小组利用实验,探究二氧化碳、氢氧化钠的性质.
化学兴趣小组利用实验,探究二氧化碳、氢氧化钠的性质.【实验探究一】小李同学用注射器吸取10mL水,再吸取10mL二氧化碳气体(此时注射器活塞位于20mL刻度处);然后密封针筒,振荡,活塞最终停在10mL刻度处.伤处实验现象说明,1体积水中通常可以溶解1体积的二氧化碳气体.
【实验探究二】小王同学将充满二氧化碳气体的试管,倒立在氢氧化钠的溶液中,试管内液面会上升.于是,他认为二氧化碳气体与氢氧化钠溶液发生了化学反应.你认为,该实验的结论不正确(填正确或不正确).
【实验探究三】小陈同学设计了如图实验装置,他将5mL氢氧化钠溶液推入集气瓶内,立即有70mL酒精缓缓流入集气瓶中.已知:①酒精在该实验中不能溶解任何物质,也不参与任何化学反应;②5mL氢氧化钠溶液中约含5mL水;③CaCI2溶液显中性,且CaCl2+Na2CO3=2NaCl+CaCO3↓.
(1)该实验能(填能或不能)确认二氧化碳气体和氢氧化钠发生了化学反应,理由是流入集气瓶中的酒精远远多于5mL.二氧化碳气体与氢氧化钠溶液反映的化学方程式是CO2+2NaOH=Na2CO3+H2O.
(2)上述实验后,集气瓶里的溶液中含有哪些溶质呢?
猜想①:酒精和氢氧化钠;猜想②:酒精和碳酸钠;猜想③:酒精、氢氧化钠和碳酸钠.
(3)为了验证猜想,他们设计了如下的实验方案:
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量溶液,滴入 过量(填少量或过量)的CaCl2 | 产生白色沉淀 | 猜想① 错误 |
| b.向步骤a中的上层清液里,滴入酚酞试液 | 若溶液变红 | 则猜想③ 成立 |
| 选项 | A | B | C | D |
| 类别 | 单质 | 构成物质微粒 | 有机化合物 | 常见的碱 |
| 物质 | 氧气、臭氧 | 分子、原子、离子 | 甲烷、乙醇 | 烧碱、纯碱 |
| A. | A、 | B. | B | C. | C | D. | D |
| A. |  过滤 | B. |  将NaOH倒入量筒中配制溶液 | ||
| C. |  加热液体 | D. |  加碱研磨后闻气味鉴别铵态氮肥 |
 某校化学兴趣小组在实验室发现了一瓶标签受到腐蚀的溶液(如图),他们对该溶液是什么产生了兴趣.
某校化学兴趣小组在实验室发现了一瓶标签受到腐蚀的溶液(如图),他们对该溶液是什么产生了兴趣.
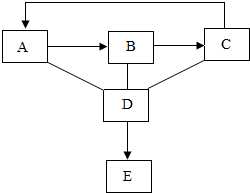 A、B、C、D、E为初中化学常见五种(酸、碱、盐、氧化物、单质)不同类别的物质,它们之间的关系如图所示(“-”表示相连的物质间能发生反应,“→”表示一种物质转化成另一种物质.反应条件、部分反应物和生成物已略去).反应C→A为化合反应,且在反应过程中放出大量热,D是人体胃液中的一种酸,请回答下列问题:
A、B、C、D、E为初中化学常见五种(酸、碱、盐、氧化物、单质)不同类别的物质,它们之间的关系如图所示(“-”表示相连的物质间能发生反应,“→”表示一种物质转化成另一种物质.反应条件、部分反应物和生成物已略去).反应C→A为化合反应,且在反应过程中放出大量热,D是人体胃液中的一种酸,请回答下列问题: