题目内容
14.化学是以实验为基础的学科,根据如图所示的实验回答问题:
(1)甲、乙两个实验中都涉及的反应原理是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(2)甲是验证化学反应前后质量守恒的实验,反应结束后天平的指针偏右,该反应是否遵守质量守恒定量是(选填“是”或“否”).
(3)乙是灭火器原理示意图,其灭火原理是隔绝空气,利用二氧化碳不燃烧,不支持燃烧的化学性质.
分析 (1)甲、乙两个实验中都涉及到盐酸与碳酸钠反应生.
(2)根据反应生成气体且反应在敞口容器进行反应分析;
(3)根据灭火的原理:清除可燃物或使可燃物与其他物品隔离、绝氧气或空气、使温度降到可燃物的着火点以下,结合泡沫灭火器成分进行解答.
解答 解:(1)盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(2)由于装置是敞口的装置,碳酸钙和稀盐酸反应产生的二氧化碳从烧杯中逸出,总质量减少,所以天平不平衡,反应结束后天平的指针将偏右;化学反应都遵守质量守恒定律,该反应遵守质量守恒定律;
故填:是.
(3)根据灭火的原理可知,泡沫灭火器的灭火原理主要是利用碳酸钠与浓盐酸生成二氧化碳的密度大于空气的密度物理性质,和二氧化碳不燃烧,不支持燃烧的化学性质,覆盖在可燃物表面,隔绝空气,进而达到灭火的目的.
故填:隔绝空气;不燃烧,不支持燃烧.
点评 要验证质量守恒定律需根据反应物的状态和产物的状态选择敞口或密闭装置,若有气体参加或生成的反应需在密闭容器中进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.如图为A、B、C为三种物质的溶解度曲线,下列说法正确的是( )
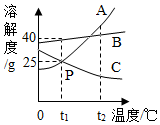

| A. | A和C的溶解度相等 | |
| B. | t2℃时,将A和C的混合溶液(两者均已达到饱和)降温至t1℃,析出晶体含有A和C | |
| C. | t2℃时,将A、B、C的饱和溶液分别降温至t1℃,所得溶液中溶质质量分数的大小关系是B>A>C | |
| D. | t1℃时,欲用A的饱和溶液配制10%的A溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器 |
5.如图为甲、乙两种物质的溶解度曲线,下列说法正确的是( )


| A. | t1℃时30g甲物质放入50g水中充分溶解所得溶液质量80g | |
| B. | 甲中含有少量的乙,可以用蒸发溶剂的方法提纯甲 | |
| C. | t2℃时,乙饱和溶液中溶质的质量分数一定小于甲饱和溶液中溶质的质量分数 | |
| D. | t2℃时,将等质量的甲、乙两种物质的溶液分别降温至t1℃,析出晶体的质量甲一定大于乙 |
2.下列有关油脂的叙述正确的是( )
| A. | 油脂一般不易溶于水 | |
| B. | 葡萄糖不能转化为人体内的脂肪 | |
| C. | 汽油、煤油、菜籽油、花牛油都属于油脂 | |
| D. | 洗发剂洗去头发上的油脂不属于乳化现象 |
19.下列实验操作正确的是( )
| A. |  检验氢气的纯度 | B. |  用镊子取用碳酸钠粉末 | ||
| C. |  用活性炭净水时上端进水 | D. |  用广口瓶贮存少量氧气 |
6.对下列事实的解释正确的是( )
| 选项 | 事 实 | 解 释 |
| A | 铜质的电线冬天直而夏天弯垂 | 原子随温度的升高而变大,随温度的降低而变小 |
| B | 分离液态空气制氧气是物理变化 | 分子种类不变 |
| C | 酒精和水混合后总体积小于二者体积之和 | 分子不断运动 |
| D | 一滴水中大约有1.67×1021个水分子 | 分子间有间隔 |
| A. | A C | B. | B | C. | C | D. | D |
 如图是氧、硫、氯三种元素的原子结构示意图
如图是氧、硫、氯三种元素的原子结构示意图