题目内容
如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:(1)硫酸的相对分子质量______,硫酸中H、S、O元素的质量比______.

(2)欲配制200g溶质质量分数为20%的稀硫酸,需用这种浓硫酸的体积是______;需加水的质量是______ (保留一位小数).
【答案】分析:(1)根据相对分子质量为各元素相对原子质量的和来计算硫酸的相对分子质量即可;利用各元素质量比为各元素相对原子质量和的比来计算硫酸中H、S、O元素的质量比即可;
(2)使用98%的浓硫酸配制20%的稀硫酸需要进行加水稀释,加水稀释前后溶质硫酸的质量不变;根据溶质质量不变,由稀硫酸的质量可计算配制时所需要浓硫酸的质量和水的质量;再根据V=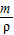 可以计算出浓硫酸的体积.
可以计算出浓硫酸的体积.
解答:解:(1)硫酸的化学式为:H2SO4,则硫酸的相对分子质量为:1×2+32+16×4=98;
硫酸中H、S、O元素的质量比为:(1×2):32:(16×4)=1:16:32.
(2)解:设需要98%的硫酸的质量为x,
根据稀释前后溶质的质量不变可得:
200g×20%=x×98%
解得:x≈40.8g;
需要水的质量为:稀释后溶液质量-稀释前溶液的质量=200g-40.8g=159.2g;
根据V=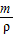 可得:需要浓硫酸的体积为:
可得:需要浓硫酸的体积为: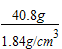 =22.2mL.
=22.2mL.
故答案为:(1)98,1:16:32;
(2)22.2mL,159.2g.
点评:此题主要考查了相对分子质量和元素质量比德计算以及溶液在稀释时溶质质量前后不变来计算.
(2)使用98%的浓硫酸配制20%的稀硫酸需要进行加水稀释,加水稀释前后溶质硫酸的质量不变;根据溶质质量不变,由稀硫酸的质量可计算配制时所需要浓硫酸的质量和水的质量;再根据V=
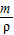 可以计算出浓硫酸的体积.
可以计算出浓硫酸的体积.解答:解:(1)硫酸的化学式为:H2SO4,则硫酸的相对分子质量为:1×2+32+16×4=98;
硫酸中H、S、O元素的质量比为:(1×2):32:(16×4)=1:16:32.
(2)解:设需要98%的硫酸的质量为x,
根据稀释前后溶质的质量不变可得:
200g×20%=x×98%
解得:x≈40.8g;
需要水的质量为:稀释后溶液质量-稀释前溶液的质量=200g-40.8g=159.2g;
根据V=
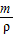 可得:需要浓硫酸的体积为:
可得:需要浓硫酸的体积为: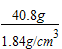 =22.2mL.
=22.2mL.故答案为:(1)98,1:16:32;
(2)22.2mL,159.2g.
点评:此题主要考查了相对分子质量和元素质量比德计算以及溶液在稀释时溶质质量前后不变来计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:
| 硫酸(化学纯) 化学式:H2SO4 相对分子质量: 密度:1.84g/cm3 质量分数:98%(1)硫酸中H、S、O原子个数比为 2:1:4 2:1:4 .(2)硫酸中H、O元素的质量比 1:32 1:32 .(3)欲用这种98%的浓硫酸200g配制溶质质量分数为24.5%的稀硫酸,需加水的质量是 150 150 g.
如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:
|

 (2010?崇明县一模)如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:
(2010?崇明县一模)如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算: