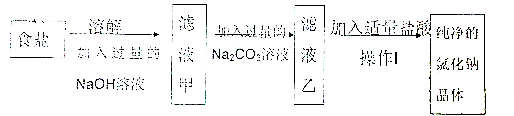题目内容
3.实验室常用下图所示的装置制取气体和气体性质的验证,请回答: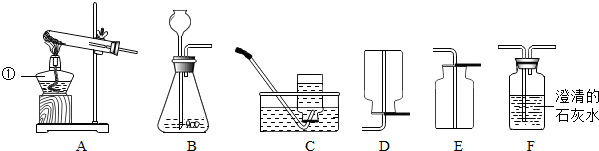
(1)仪器①的名称酒精灯.
(2)实验室用过氧化氢制取氧气,可选取的装置是BC(或BE)(填序号),发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)用B、F制取二氧化碳并验证性质,F装置中发生反应的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O.
(4)某同学利用石灰石和盐酸通过装置B、F来验证二氧化碳的性质,实验过程中观察到F中有气泡冒出,澄清的石灰水未变浑浊,试分析其可能的原因盐酸浓度大.
分析 (1)据常用仪器的名称和用途解答;
(2)制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热;
(3)根据题目中的信息,已知反应物和生成物,再根据质量守恒定律,配平化学方程式.
(4)从盐酸具有挥发性的角度来分析.
解答 解:(1)图中①是酒精灯;
(2)如果用双氧水制氧气就不需要加热,发生装置选择B;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;反应的方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)用B、F制取二氧化碳并验证性质,F装置中发生反应的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O;
(4)若二氧化碳气体不能使石灰水变浑浊,可能是盐酸浓度过大挥发出氯化氢气体,与氢氧化钙发生了反应.
故答案为:(1)酒精灯; (2)BC(或BE)、2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)盐酸浓度大.
点评 本题考查气体的收集装置、化学方程式的书写、盐酸的性质等知识点,需要同学们在掌握基本知识的基础上灵活作答.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
12.将一定量的锌粉加入到硫酸亚铁、硫酸铜和硫酸镁的混合溶液中,过一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述正确的是( )
①滤渣中一定含有锌
②滤渣中一定含有铜,可能含有锌
③向滤渣中加入稀盐酸,最后溶液一定变成浅绿色
④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色.
①滤渣中一定含有锌
②滤渣中一定含有铜,可能含有锌
③向滤渣中加入稀盐酸,最后溶液一定变成浅绿色
④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色.
| A. | ①④⑤ | B. | ②④ | C. | ②③④ | D. | ②③④⑤ |
13.许多物质在溶液中都以离子形式存在.我们熟悉的复分解反应就是溶液中离子间结合得到水、气体或沉淀 的一类化学反应.如:氢氧化钠与盐酸的反应就是溶液中的H+和OH-结合成水分子的过程,你认为下列各组离子间不能反应的是( )
| A. | H+ Na+ 0H- NO3- | B. | Na+ K+Cl-OH- | ||
| C. | H+ K+CO32- HCO3- | D. | K+ Ba2+ Cl- SO42- |