题目内容
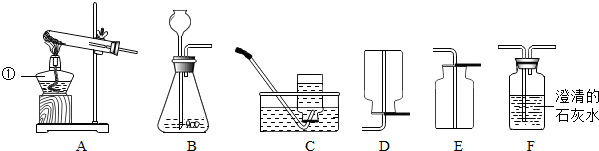
11.在学习质量守恒定律的内容时,我们曾经做了如下图所示的实验,请回忆当时的情景回答下列问题:
(1)图甲中反应后天平的指针偏右(“偏左”“偏右”“不变”),原因是反应生成的二氧化碳扩散到空气中,该反应是否符合质量守恒定律?符合.(“符合”或“不符合”)
(2)图乙中在实验设计时,玻璃管上方系一瘪气球的目的是燃烧时瓶内气体受热膨胀,压强增大,防止塞子被弹起(或为了减压,防止塞子被弹起);.图中发生的化学反应方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)由质量守恒定律可知,化学反应前后,一定改变的是③(填序号).
①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质总质量.
分析 化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和;
化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答 解:(1)反应停止后,可观察到甲天平不平衡,该反应符合质量守恒定律,天平不平衡的原因是碳酸钠和稀盐酸反应生成的二氧化碳扩散到了空气中,反应后天平的指针.
故填:偏右;反应生成的二氧化碳扩散到空气中;符合.
(2)图乙中在实验设计时,玻璃管上方系一瘪气球的目的是:燃烧时瓶内气体受热膨胀,压强增大,防止塞子被弹起(或为了减压,防止塞子被弹起);
磷和氧气在点燃的条件下生成五氧化二磷,配平即可,则化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
答案:燃烧时瓶内气体受热膨胀,压强增大,防止塞子被弹起(或为了减压,防止塞子被弹起);4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)由质量守恒定律可知,化学反应前后,一定不变的是原子种类、原子数目、元素种类、物质总质量;一定改变的是分子种类.
故填:③.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
相关题目
12.实验室制氧气不能选用的药品是( )
| A. | 加热氯酸钾和二氧化锰 | B. | 加热高锰酸钾 | ||
| C. | 双氧水和二氧化锰 | D. | 分解氧化汞 |
13.下列有关物质的性质中,属于化学性质的是( )
| A. | 铜具有优良的导电性 | |
| B. | 常温下水是一种无色无味的液体 | |
| C. | 氧气不易溶于水 | |
| D. | 镁能在空气中燃烧,生成一种白色粉末状固体 |
10.一种无色溶液中滴加氯化钡溶液,有白色沉淀生成,则该溶液一定是( )
| A. | 硝酸银 | B. | 硫酸钠 | C. | 稀硫酸 | D. | 无法确定 |
20.下列各组物质能与pH=1溶液共存,形成无色溶液的是( )
| A. | K2SO4、Ba(OH)2、KCl | B. | Cu(NO3)2、NaCl、KNO3 | ||
| C. | Na2CO3、KNO3、NH4Cl | D. | MgSO4、NaNO3、KCl |