题目内容
6.电解水实验不能证明的是( )| A. | 水是由氢、氧两种元素组成的化合物 | |
| B. | 在化学变化中,分子可分而原子不可分 | |
| C. | 化学反应前后,元素的种类不变 | |
| D. | 分子不停地运动,且分子之间有间隔 |
分析 根据电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2解答.
解答 解:A、通过电解水生成氢气和氧气,可以证明水是由氢氧两种元素组成;
B、通过电解水生成氢气和氧气,可以证明在化学变化中分子可分成原子,而原子不能再分;
C、通过电解水生成氢气和氧气,可以证明化学变化前后,元素种类不变;
D、电解水实验不能证明分子在不停地运动,且分子间有间隔.
故选:D.
点评 反应前后元素的种类不变,根据生成物的元素组成可以判断反应物的元素组成,例如生成的氢气和氧气中,含有氢元素和氧元素,可以判断反应物水中含有氢元素和氧元素.

练习册系列答案
相关题目
17.如表是某成年男子血液的化验结果.根据表中的数据回答:
(1)依据化验项目第②项判断此人有炎症,原因在于白细胞数目高出正常值.
(2)依据化验项目第①项判断此人患有贫血.请在下列四项中选择:他应该多吃含B、D丰富的食品.(可多选)
A.钙 B.铁 C.维生素B1 D.蛋白质.
| 化验项目 | 正常情况 | 化验结果 | |
| 血液 | ①血红蛋白 | 120~150克/升 | 100克/升 |
| ②白细胞 | 4×109~10×109个/升 | 16×109个/升 | |
| ③血清 | 含抗A凝集素 |
(2)依据化验项目第①项判断此人患有贫血.请在下列四项中选择:他应该多吃含B、D丰富的食品.(可多选)
A.钙 B.铁 C.维生素B1 D.蛋白质.
14.网络神曲“化学是你,化学是我”揭示了化学与生活的密切关系.下列有关说法中正确的是( )
| A. | 水是一种重要的自然资源,为节约用水,工业用水循环利用,农业采用喷灌、滴灌减少用水 | |
| B. | 碳酸钠俗名纯碱,可用于清洗厨房用具的油污 | |
| C. | 防毒面具的滤毒罐里盛放活性炭,滤毒过程发生了化学变化 | |
| D. | 厨房中处处有化学.炒菜时,燃气灶的火焰呈黄色,锅底出现黑色物质,此时需要调小灶具的进风量 |
18.Na2CO3是一种常见的盐,多角度看物质可以提高对该物质的认识.
(1)Na2CO3俗称纯碱;
(2)从类别看,Na2CO3可以看作是某种碱和某种氧化物反应的产物.该反应的化学方程式:2NaOH+CO2=Na2CO3+H2O;
(3)从用途看,Na2CO3可制备某些物质,如Na2CO3+M→NaOH+N,写出该反应的化学方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(4)从组成看,Na2CO3、NaCl均属钠盐,NaCl溶于水显中性,但Na2CO3溶于水显碱性.请完善实验方案,探析上述性质差异的初步原因:
(1)Na2CO3俗称纯碱;
(2)从类别看,Na2CO3可以看作是某种碱和某种氧化物反应的产物.该反应的化学方程式:2NaOH+CO2=Na2CO3+H2O;
(3)从用途看,Na2CO3可制备某些物质,如Na2CO3+M→NaOH+N,写出该反应的化学方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(4)从组成看,Na2CO3、NaCl均属钠盐,NaCl溶于水显中性,但Na2CO3溶于水显碱性.请完善实验方案,探析上述性质差异的初步原因:
| 实验步骤 | 实现现象 | 实验结论 |
| 取适量NaCl溶液于试管中,滴加石蕊试液,振荡 | ①无明显现象 | Na+和Cl-与溶液的酸碱性无关 |
| 取适量滴有酚酞试液的Na2CO3溶液少许于试管中,滴加②过量CaCl2(BaCl2等)溶液 | ③产生白色沉淀,溶液红色消失 | ④Na2CO3溶于水呈碱性与CO32-有关 |
15.甲醛(化学式是CH2O)是一种无色、有刺激性气味的气体,易溶于水,有毒,生产上可以作为防腐剂,在生产服装布料的过程中加入甲醛可使服装达到防皱效果.下列有关甲醛的说法错误的是( )
| A. | 甲醛是有机物 | |
| B. | 可以用甲醛浸泡海鲜防腐 | |
| C. | 组成甲醛的碳、氢、氧元素的质量比为6:1:8 | |
| D. | 若买回的服装中有残留甲醛,可用水洗去 |
8.碳元素与氧元素的本质区别是( )
| A. | 原子的电子层数不同 | B. | 原子的中子数不同 | ||
| C. | 原子的质子数不同 | D. | 原子的最外层电子数不同 |
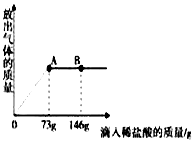 在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题:
在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题: