题目内容
3.某兴趣小组的同学用生铁制成的铁钉来制取晶体[FeSO4•7H2O],进行了如图实验: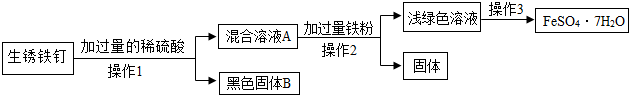
(1)操作1、2中所用的玻璃仪器有玻璃棒、烧杯、胶头滴管和漏斗.
(2)混合溶液A中的溶质有Fe2(SO4)3、H2SO4和FeSO4(化学式).
(3)操作3的步骤是加热浓缩、冷却结晶、过滤、洗涤、干燥.
(4)洗涤[FeSO4•7H2O]晶体可下列试剂C.
A.水 B.稀硫酸 C.冷水.
分析 (1)操作1、2分别是使固体与溶液反应、分离固体和液体,即进行过滤操作,进行分析解答.
(2)混合溶液A,是生铁的铁钉与过量稀硫酸反应得到的,铁锈的主要成分氧化铁与稀硫酸反应生成硫酸铁和水,铁与稀硫酸反应生成硫酸亚铁和氢气,据此进行分析解答.
(3)操作3是从硫酸亚铁溶液中制得FeSO4•7H2O,进行分析解答.
(4)
解答 解:(1)操作1、2分别是使固体与溶液反应、分离固体和液体,即进行过滤操作;使固体与溶液反应,在烧杯中进行,用胶头滴管滴加稀硫酸,用玻璃棒进行搅拌;进行过滤操作,所用的玻璃仪器是漏斗、烧杯、玻璃棒;故操作1、2中所用的玻璃仪器有玻璃棒、烧杯、胶头滴管和漏斗.
(2)混合溶液A,是生铁的铁钉与过量稀硫酸反应得到的,铁锈的主要成分氧化铁与稀硫酸反应生成硫酸铁和水,铁与稀硫酸反应生成硫酸亚铁和氢气,则混合溶液A中的溶质有Fe2(S04)3、H2SO4和FeSO4.
(3)操作3是从硫酸亚铁溶液中制得FeSO4•7H2O,操作3的步骤是加热浓缩、冷却结晶、过滤、洗涤、干燥.
(4)硫酸亚铁的溶解度随着温度的升高而增大,冷水的温度低,硫酸亚铁的溶解度小,洗涤[FeSO4•7H2O]晶体可用冷水.
故答案为:(1)漏斗;(2)FeSO4;(3)冷却结晶;(4)C.
点评 本题难度不大,理解生铁制成的铁钉来制取FeSO4•7H2O的流程,掌握金属的化学性质、过滤所需的仪器等是正确解答本题的关键.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
16.下列实验设计能达到实验目的是( )


| A. | 图1探究可燃物燃烧的条件 | B. | 图2探究分子运动现象 | ||
| C. | 图3验证甲烷燃烧生成CO2和H2O | D. | 图4探究质量守恒定律 |
14.人们在工作、生活中的下列做法不安全的是( )
| A. | 液化石油气泄露时,立即关闭气瓶阀门并开窗通风 | |
| B. | 霉变的花生先用水漂洗,再煮熟后食用 | |
| C. | 酒精灯内的酒精洒出燃烧时,立即用湿抹布盖灭 | |
| D. | 燃放烟花爆竹时远离人群和可燃物 |
8.从如图所示实验中得出的结论不合理的是( )


| A. | 甲实验可比较锌、铁的活动性 | |
| B. | 乙实验说明通电导线周围存在磁场 | |
| C. | 丙实验说明压力一定时,压力的作用效果与受力面积有关 | |
| D. | 丁实验说明铁生锈需要有水 |
15.4.6g乙醇与一定质量的氧气不完全反应,生成了4.4g的CO2和5.4g的H2O和一定质量的CO,下列说法正确的是( )
| A. | 生成CO的质量为5.6g | |
| B. | 参加反应的乙醇和氧气的系数比为1:3 | |
| C. | 该反应不遵守质量守恒定律 | |
| D. | 参加反应的氧气的质量为8g |
13.下列物质属于纯净物的是( )
| A. | 石灰石 | B. | 石油 | C. | 蒸馏水 | D. | 天然气 |
 化学课上我们曾经观察过如图所示的实验.
化学课上我们曾经观察过如图所示的实验.