题目内容
7.合金是重要的金属材料.(1)下列物品所使用的主要材料属于合金的是cd(填字母序号).
a.青花瓷瓶 b.橡胶充气艇 c.不锈钢锅 d.铝窗
(2)黄铜是铜锌合金,黄铜渣中约含 Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质.处理黄铜渣可得到硫酸锌,其主要流程如图(杂质不溶于水、不参与反应):
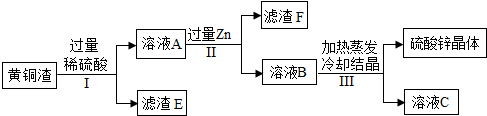
①写出步骤Ⅰ中反应的化学方程式(要求写出2种反应,反应类型相同的看作同一种反应)为H2SO4+Zn═ZnSO4+H2↑;ZnO+H2SO4═ZnSO4+H2O或CuO+H2SO4═CuSO4+H2O.
②步骤Ⅱ中加入过量Zn的目的是除去过量的稀硫酸和CuSO4.
③下列说法正确的是ab
a.Ⅰ、Ⅱ、III中的操作均包含过滤
b.溶液A中ZnSO4 的质量大于CuSO4
c.溶液C中溶质的质量分数小于溶液B
④你认为滤渣E和F应该如何处理:回收,用于提取金属铜.
分析 (1)合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质;合金具有以下特点:①一定是混合物;②合金中至少有一种金属等.
(2)①根据合金的定义解答;
②根据溶液A的成分和锌的性质解答;
③根据金属与酸、盐的溶液反应的规律进行分析解答.
④根据滤渣的成分解答.
解答 解:(1)a、青花瓷瓶是用泥土烧制而成的,属于无机非金属材料,故选项错误.
b、橡胶充气艇是用合成橡胶制成的,合成橡胶属于三大合成材料之一,故选项错误.
c、不锈钢锅是用不锈钢制成的,是铁的合金,故选项正确.
d、铝窗是用铝合金制成的,是铝的合金,故选项正确.
故选:cd;
(2)①因为黄铜渣中约含 Zn、ZnO、Cu、CuO,其中除铜外均可与稀硫酸反应,步骤Ⅰ中化学方程式有H2SO4+Zn═ZnSO4+H2↑、ZnO+H2SO4═ZnSO4+H2O、CuO+H2SO4═CuSO4+H2O;
②步骤Ⅱ中加入过量Zn的目的是除去过量的稀硫酸和操作一生成的CuSO4;
③由图可知,操作Ⅰ过滤后得铜,操作Ⅱ过滤是除去锌,操作III过滤是去除结晶得到的硫酸锌晶体,故a正确;
因氧化锌的质量大于氧化铜,另外锌也能和硫酸反应生成硫酸锌,而铜和硫酸不反应,故溶液A中硫酸锌的质量大于硫酸铜,故b正确;
溶液B是硫酸锌的不饱和溶液,蒸发结晶后析出硫酸锌晶体,得到的溶液C是硫酸锌的饱和溶液其溶质质量分数大于溶液B,故c错误;
④滤渣E和F中都很有铜,所以回收,用于提取金属铜.
故答案为:(1)cd
(2)①H2SO4+Zn═ZnSO4+H2↑;ZnO+H2SO4═ZnSO4+H2O 或CuO+H2SO4═CuSO4+H2O
②CuSO4 ③a b
④回收,用于提取金属铜
点评 本题重点考查了合金的相关知识及金属活动性顺序及其应用,了解相关知识即可正确解答.

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案| A. | 用盐酸除去石灰水中的少量CaCO3 | B. | 用盐酸验证久置的NaOH溶液已变质 | ||
| C. | 用燃着的木条区分O2和CO2 | D. | 用盐酸除去铁钉表面的少量铁锈 |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向醋酸中加入氢氧化钠溶液 | 无明显现象 | 二者之间不发生反应 |
| B | 向溶质质量分数为5%的过氧化氢溶液中加入少量氧化铜 | 有大量气泡产生 | 氧化铜起催化作用 |
| C | 将两根铜丝分别伸入硫酸铝溶液和硝酸银溶液中 | 伸入硝酸银溶液中的铜丝上有白色固体附着,另一根铜丝无变化 | 金属活动性顺序为 Al>Cu>Ag |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是H2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 硬度比铝大 | B. | 可溶于水 | C. | 具有导电性 | D. | 具有可燃性 |

下列说法不正确的是( )
| A. | 步骤②中发生化合反应、置换反应和复分解反应 | |
| B. | “滤液1”中一定含FeCl2,一定不含CuCl2 | |
| C. | 步骤④反应为:2M+2FeCl2+H2O2=2FeCl3+2H2O,M是HCl | |
| D. | 若滤渣也为m1g,则废液中FeCl3与CuCl2的质量比为65:56 |
| A. | 液氮用作冷冻剂 | B. | 干冰用于人工降雨 | ||
| C. | 氢气用于填充探空气球 | D. | 熟石灰用于改良酸性土壤 |
| A. | 水(H2O)m(H):m(O)=1:2 | B. | 乙炔(C2H2) m(C):m(H)=2:1 | ||
| C. | 氨气(NH3)m(N):m(H)=14:1 | D. | 三氧化硫(SO3) m(S):m(O)=2:3 |
