题目内容
5. 如今,走向“地铁、高铁时代”的中国,正大力发展电气化铁路.高铁的运行为我们的出行提供了方便.中国的高铁技术不仅服务于中国,也终将造福于全人类.请试着回答下列问题:
如今,走向“地铁、高铁时代”的中国,正大力发展电气化铁路.高铁的运行为我们的出行提供了方便.中国的高铁技术不仅服务于中国,也终将造福于全人类.请试着回答下列问题:(1)地铁、高铁的车身可能是B;(在A、B、C中选填)
A.韧性好、硬度大的锰钢B.抗腐蚀、密度小的铝合金C.抗腐蚀性好的不锈钢
(2)高铁在工作过程中的能量转化为电能转化为机械能;
(3)高铁运行时的接触材料用铜及铜合金线,而火法炼铜是当今生产铜的主要方法.其中重要的一步是用氧化亚铜(Cu2O)和硫化亚铜(Cu2S)高温反应生成高纯度的铜和一种气态空气污染物,则发生反应的化学方程式是2Cu2O+Cu2S$\frac{\underline{\;高温\;}}{\;}$6Cu+SO2↑,该反应的反应物中铜元素的化合价分别为+1、+1.
分析 (1)根据合金的性质以及车身对材料的要求来分析;
(2)根据能量的转化来分析;
(3)根据反应物和生成物以及反应条件书写化学方程式,并根据正负化合价代数和为零计算元素的化合价.
解答 解:(1)车身要求合金材料抗腐蚀、密度小;故填:B;
(2)地铁机车通常是电力机车,机车行驶过程中的能量转化是电能转化为机械能;故填:电能转化为机械能;
(3)根据题干信息以及元素守恒可知,还生成二氧化硫气体.在化合物中各元素正负化合价的代数和为零,氧化亚铜(Cu2O)中,氧元素显-2价,故其中铜元素显+1价;硫化亚铜(Cu2S)中,硫元素显-2价,故其中铜元素显+1价.故填:2Cu2O+Cu2S$\frac{\underline{\;高温\;}}{\;}$6Cu+SO2↑;+1、+1.
点评 本题考查了金属材料的应用,完成此题,可以依据题干提供的信息进行,书写反应的化学方程式要注意配平.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
16.推理是一种重要的学习方法.下列推理中正确的是( )
| A. | 有机物都含有碳元素,含碳元素的化合物都是有机物 | |
| B. | 氧化物都含有氧元素,则含有氧元素的化合物一定是氧化物 | |
| C. | 酸碱盐之间的复分解反应一定有盐生成,则有盐生成的反应一定是酸碱盐之间的复分解反应 | |
| D. | 分子、原子都是不带电的微粒,但不带电的微粒不一定都是分子、原子 |
20.如图是提纯CO、CO2混合气体中的CO并还原氧化铁的示意图.请回答有关问题:
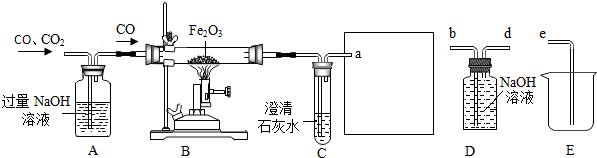
(1)为避免CO污染空气,并回收利用CO,方框中连接的是D和E,导管接口的连接顺序为a→d→b→e.D装置中NaOH的作用是除去残余的CO2.如果导管连接错误,后果是CO排入空气中污染空气.
(2)实验进行一段时间后,B装置的玻璃管中的现象为固体由红棕色变成黑色,反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.用这种方法“炼”得的铁与工业上炼出的生铁在组成上的最大区别是“炼”得的铁不含碳,工业上的生铁含有碳.
(3)实验结束后,要从A装置的混合溶液中回收得到较纯净的NaOH固体.
资料显示,在不同温度下NaOH的溶解度如下:
利用实验室的试剂和条件,实验步骤如下(其中Ⅰ、Ⅱ、Ⅲ为实验操作):
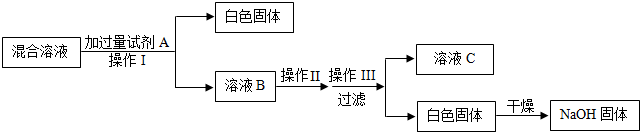
请回答下列问题:
①化学式:A.Ca(OH)2;
②操作名称:Ⅲ.冷却(或降温结晶);
③如果在操作Ⅱ的过程中,溶液B中出现少量浑浊,原因可能是Ca(OH)2的溶解度随温度升高而降低,从溶液B中析出,形成浑浊.

(1)为避免CO污染空气,并回收利用CO,方框中连接的是D和E,导管接口的连接顺序为a→d→b→e.D装置中NaOH的作用是除去残余的CO2.如果导管连接错误,后果是CO排入空气中污染空气.
(2)实验进行一段时间后,B装置的玻璃管中的现象为固体由红棕色变成黑色,反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.用这种方法“炼”得的铁与工业上炼出的生铁在组成上的最大区别是“炼”得的铁不含碳,工业上的生铁含有碳.
(3)实验结束后,要从A装置的混合溶液中回收得到较纯净的NaOH固体.
资料显示,在不同温度下NaOH的溶解度如下:
| 温度/℃ | 10 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/(g/100g水) | 64 | 85 | 138 | 203 | 285 | 376 |

请回答下列问题:
①化学式:A.Ca(OH)2;
②操作名称:Ⅲ.冷却(或降温结晶);
③如果在操作Ⅱ的过程中,溶液B中出现少量浑浊,原因可能是Ca(OH)2的溶解度随温度升高而降低,从溶液B中析出,形成浑浊.
15.类推是学习化学的一种重要方法,下列正确的是( )
| A. | 离子是带电的粒子,所以带电的粒子一定是离子 | |
| B. | 燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 | |
| C. | 点燃氢气、甲烷前需验纯,所以点燃任何可燃性气体前都需验纯 | |
| D. | 燃烧过程伴随发光、放热现象,所以有发光、放热现象的变化都是燃烧 |
 A、B、C、D、E为五种不同类别的纯净物,他们之间的反应关系如图.“”表示两种物质之间能相互转化,“-”表示两物质之间能发生化学反应.其中,A为金属单质,B为赤铁矿的主要成分,E的水溶液为黄色.请回答:
A、B、C、D、E为五种不同类别的纯净物,他们之间的反应关系如图.“”表示两种物质之间能相互转化,“-”表示两物质之间能发生化学反应.其中,A为金属单质,B为赤铁矿的主要成分,E的水溶液为黄色.请回答: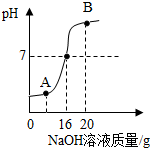 实验室测定一瓶稀硫酸中溶质的质量分数,取10g该待测液,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,加入氢氧化钠溶液的质量与溶液pH的变化关系如图所示.请根据题意填空并计算:
实验室测定一瓶稀硫酸中溶质的质量分数,取10g该待测液,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,加入氢氧化钠溶液的质量与溶液pH的变化关系如图所示.请根据题意填空并计算: