题目内容
14.除去泥沙的粗盐样品中还有少量的Na2SO4、MgCl2、CaCl2等可溶性杂质,小青同学设计了以下实验方案来除去粗盐中的可溶性杂质.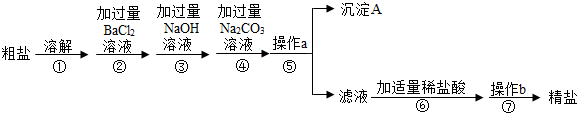
请根据如图回答下列问题:
(1)操作a的名称是过滤.操作b中要使用到玻璃棒,其作用是搅拌,防止液体局部受热,造成液滴飞溅.
(2)沉淀A中所包含的物质有氢氧化镁,碳酸钡,碳酸钙,硫酸钡.
(3)步骤④的目的是除去氯化钙和氯化钡.
(4)步骤⑥的目的是除去氢氧化钠和碳酸钠.
分析 掌握粗盐提纯的步骤是溶解、过滤、蒸发,了解玻璃棒的作用;
欲除去溶液的MgCl2、CaCl2、Na2SO4,则用氢氧化镁除掉氯化镁,用氯化钡除掉硫酸钠,用碳酸钠除掉氯化钙与多余的氯化钡;在滤液中加盐酸的作用,应考虑除去NaOH、Na2CO3溶液.
解答 解:(1)第a步操作步骤的名称是过滤.在操作b是蒸发,要用玻璃棒,作用是搅拌,防止液体局部受热,造成液滴飞溅.
(2)欲除去溶液中的MgCl2、CaCl2、Na2SO4,则用氢氧化钠除掉氯化镁生成氢氧化镁沉淀,用氯化钡除掉硫酸钠生成硫酸钡沉淀,用碳酸钠除掉氯化钙与多余的氯化钡生成碳酸钡和碳酸钙沉淀,正确滴加顺序依次为:过量的NaOH溶液、过量氯化钡溶液、过量碳酸钠溶液.第②步操作的目的是除去粗盐中的Na2SO4;
(3)步骤④用碳酸钠除掉氯化钙与多余的氯化钡,加盐酸可以跟氢氧化钠和过量的碳酸钠反应,
(4)第⑥步操作的目的是除去滤液中的除去NaOH、Na2CO3溶液.
答案:(1)过滤;搅拌,防止液体局部受热,造成液滴飞溅;
(2)氢氧化镁,碳酸钡,碳酸钙,硫酸钡;
(3)除去氯化钙和氯化钡;
(4)除去氢氧化钠和碳酸钠.
点评 掌握氯化钠与粗盐的提纯的方法及其注意事项;掌握一定溶质质量分数的溶液的配制方法;了解除杂和净化的方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.化学兴趣小组的同学做的下列家庭小实验中,主要发生物理变化的是( )
| A. | 用蜡烛制取炭黑 | B. | 用简易净水器净水 | ||
| C. | 自制汽水 | D. | 鸡蛋壳加入食醋中 |
2.如图是甲、乙三种固体物质的溶解度曲线.下列叙述不正确的是( )
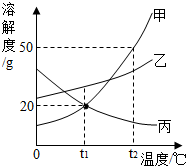

| A. | t1℃,甲和丙的溶解度均为20g | |
| B. | t2℃,物质甲的饱和溶液溶质的质量分数为50% | |
| C. | 将t2℃时丙的饱和溶液降温至t1℃,溶质的质量分数不变 | |
| D. | 加水或升温均可使乙的饱和溶液变为不饱和溶液;甲中含有少量乙,可用冷却热饱和溶液的方法提纯甲 |
9.谚语诗词中蕴含着科学道理,下列说法正确的是( )
| A. | “真金不怕火炼”是说黄金熔点很高 | |
| B. | “百炼成钢”与“只要功夫深铁杵磨成针”蕴含的化学原理相同 | |
| C. | “釜底抽薪”是一种灭火方法,其灭火的原理是清除可燃物 | |
| D. | “众人拾柴火焰高”是指可燃物越多,其着火点就越低,约容易燃烧 |
3.把A、B、C、D四种纯净物放在一密闭容器中,在一定条件下充分反应,反应前后各物质的质量如下表:
回答下列问题:
(1)反应后D的质量是10g;
(2)C物质可能是催化剂(填写反应物、生成物或催化剂);
(3)容器中发生反应的反应类型是分解反应(填写基本反应类型).
| 物质 | A | B | C | D |
| 反应前质量/g | 2 | 25 | 2 | 1 |
| 反应后质量/g | 18 | 0 | 2 | 未知 |
(1)反应后D的质量是10g;
(2)C物质可能是催化剂(填写反应物、生成物或催化剂);
(3)容器中发生反应的反应类型是分解反应(填写基本反应类型).
4.下列关于分子的说法错误的是( )
| A. | “八月桂花香”说明分子不断运动着 | |
| B. | 气体受热膨胀是因为气体分子体积变大 | |
| C. | 100mL酒精和100mL水混合小于200mL,说明分子之间有间隔 | |
| D. | 分子是保持物质化学性质的唯一粒子 |
 如今,走向“地铁、高铁时代”的中国,正大力发展电气化铁路.高铁的运行为我们的出行提供了方便.中国的高铁技术不仅服务于中国,也终将造福于全人类.请试着回答下列问题:
如今,走向“地铁、高铁时代”的中国,正大力发展电气化铁路.高铁的运行为我们的出行提供了方便.中国的高铁技术不仅服务于中国,也终将造福于全人类.请试着回答下列问题: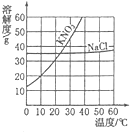 根据如图中KNO3和NaCI两种物质的溶解度曲线,回答下列问题.
根据如图中KNO3和NaCI两种物质的溶解度曲线,回答下列问题.