题目内容
13.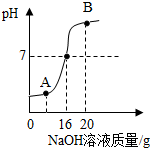 实验室测定一瓶稀硫酸中溶质的质量分数,取10g该待测液,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,加入氢氧化钠溶液的质量与溶液pH的变化关系如图所示.请根据题意填空并计算:
实验室测定一瓶稀硫酸中溶质的质量分数,取10g该待测液,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,加入氢氧化钠溶液的质量与溶液pH的变化关系如图所示.请根据题意填空并计算:(1)20g8%的氢氧化钠溶液中所含溶质的质量是1.6g.
(2)B点对应的溶液中含有的溶质是NaOH、Na2SO4.
(3)计算待测液中溶质的质量分数.(精确到0.1%)
分析 根据氢氧化钠溶液质量、溶质质量分数可以计算氢氧化钠溶液中溶质的质量;
氢氧化钠和稀硫酸反应生成硫酸钠和水,根据恰好完全反应时消耗氢氧化钠溶液的质量可以计算反应的硫酸质量,进一步可以计算待测液中溶质的质量分数.
解答 解:(1)20g8%的氢氧化钠溶液中所含溶质的质量是:20g×8%=1.6g,
故填:1.6.
(2)B点对应的溶液中含有反应生成的硫酸钠和过量的氢氧化钠,因此B点对应的溶液中含有的溶质是NaOH、Na2SO4.
故填:NaOH、Na2SO4.
(3)设10g稀硫酸中硫酸的质量为x,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
16g×8% x
$\frac{80}{16g×8%}$=$\frac{98}{x}$,
x=1.568g,
则待测液中溶质的质量分数为:$\frac{1.568g}{10g}$×100%=15.7%,
答:待测液中溶质的质量分数为15.7%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
4.化学兴趣小组的同学做的下列家庭小实验中,主要发生物理变化的是( )
| A. | 用蜡烛制取炭黑 | B. | 用简易净水器净水 | ||
| C. | 自制汽水 | D. | 鸡蛋壳加入食醋中 |
1.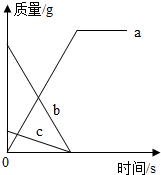 某化学反应中,各物质质量随时间变化的曲线如图所示.下列说法一定正确的是( )
某化学反应中,各物质质量随时间变化的曲线如图所示.下列说法一定正确的是( )
 某化学反应中,各物质质量随时间变化的曲线如图所示.下列说法一定正确的是( )
某化学反应中,各物质质量随时间变化的曲线如图所示.下列说法一定正确的是( )| A. | 该反应是分解反应 | |
| B. | 物质c发生了还原反应 | |
| C. | 物质b是化合物 | |
| D. | 物质a中的元素种类等于b和c中的元素种类之和 |
8.根据如图所给信息,判断下列叙述中不正确的是( )
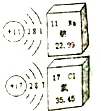

| A. | 钠原子的核内有11个质子 | |
| B. | 氯元素的相对原子质量为35.45g | |
| C. | 氯化钠是由钠离子和氯离子构成的 | |
| D. | 钠离子、氯离子的最外层都有8个电子 |
2.如图是甲、乙三种固体物质的溶解度曲线.下列叙述不正确的是( )
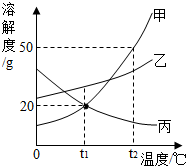

| A. | t1℃,甲和丙的溶解度均为20g | |
| B. | t2℃,物质甲的饱和溶液溶质的质量分数为50% | |
| C. | 将t2℃时丙的饱和溶液降温至t1℃,溶质的质量分数不变 | |
| D. | 加水或升温均可使乙的饱和溶液变为不饱和溶液;甲中含有少量乙,可用冷却热饱和溶液的方法提纯甲 |
3.把A、B、C、D四种纯净物放在一密闭容器中,在一定条件下充分反应,反应前后各物质的质量如下表:
回答下列问题:
(1)反应后D的质量是10g;
(2)C物质可能是催化剂(填写反应物、生成物或催化剂);
(3)容器中发生反应的反应类型是分解反应(填写基本反应类型).
| 物质 | A | B | C | D |
| 反应前质量/g | 2 | 25 | 2 | 1 |
| 反应后质量/g | 18 | 0 | 2 | 未知 |
(1)反应后D的质量是10g;
(2)C物质可能是催化剂(填写反应物、生成物或催化剂);
(3)容器中发生反应的反应类型是分解反应(填写基本反应类型).
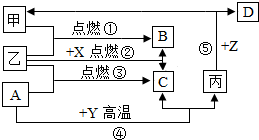 如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态.化合物D的水溶液呈浅绿色.
如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态.化合物D的水溶液呈浅绿色. 如今,走向“地铁、高铁时代”的中国,正大力发展电气化铁路.高铁的运行为我们的出行提供了方便.中国的高铁技术不仅服务于中国,也终将造福于全人类.请试着回答下列问题:
如今,走向“地铁、高铁时代”的中国,正大力发展电气化铁路.高铁的运行为我们的出行提供了方便.中国的高铁技术不仅服务于中国,也终将造福于全人类.请试着回答下列问题: