题目内容
下列图象能正确反应对应变化关系的是( )
 |
 |
 |
 |
| A.向一定量的二氧化 锰中加入过氧化氢溶液 |
B.碳在盛有氧气的 密闭容器内燃烧 |
C.向两份完全相同 的稀盐酸中分别加入锌粉、镁粉 |
D.将水通电电解一段时间 |
| A、A | B、B | C、C | D、D |
考点:催化剂的特点与催化作用,电解水实验,金属的化学性质,质量守恒定律及其应用
专题:元素化合物知识型
分析:A、二氧化锰在过氧化氢分解的过程中充当的是催化剂,可以结合催化剂的定义来完成解答;
B、炭在盛有氧气的密闭容器内燃烧,根据质量守恒定律反应前后质量不变;
C、根据氢元素的质量守恒来进行判断;
D、根据通电分解水的实验现象及结论进行解答;
B、炭在盛有氧气的密闭容器内燃烧,根据质量守恒定律反应前后质量不变;
C、根据氢元素的质量守恒来进行判断;
D、根据通电分解水的实验现象及结论进行解答;
解答:解:
A、二氧化锰在过氧化氢分解的过程中充当的是催化剂,其质量在反应前后不会改变,故A错误;
B、炭在盛有氧气的密闭容器内燃烧,根据质量守恒定律反应前后质量不变,故B错误;
C、向两份完全相同的稀盐酸中分别加入锌粉、镁粉,图中信息可知,由于镁粉和锌粉是足量的,所以产生氢气质量应该相等,故C错误;
D、通电分解水时产生氢气的体积是氧气的二倍,故D正确;
答案:D
A、二氧化锰在过氧化氢分解的过程中充当的是催化剂,其质量在反应前后不会改变,故A错误;
B、炭在盛有氧气的密闭容器内燃烧,根据质量守恒定律反应前后质量不变,故B错误;
C、向两份完全相同的稀盐酸中分别加入锌粉、镁粉,图中信息可知,由于镁粉和锌粉是足量的,所以产生氢气质量应该相等,故C错误;
D、通电分解水时产生氢气的体积是氧气的二倍,故D正确;
答案:D
点评:正确辨别坐标所表示的变化量,是解答此类问题的关键,分析变化中相关量的变化关系,是解答问题的基础.

练习册系列答案
相关题目
下列实验方案不可行的是( )
| A、用蒸馏法制取蒸馏水 |
| B、用肥皂水区分硬水和软水 |
| C、用燃着的木条区别CO2和O2 |
| D、用称取煮沸前后蒸馏水的方法来验证质量守恒定律 |
下列操作正确的是( )
| A、将浓硫酸慢慢注入水中,搅拌,冷却,置镁条于其中探究Mg的活泼性 |
| B、金属镁燃烧,用干冰灭火器灭火 |
| C、将NaOH溶液缓慢滴入MgSO4溶液中,可观察到白色沉淀生成 |
| D、将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
下列实验现象的描述正确的是( )
| A、镁在空气中燃烧,发出耀眼白光,生成白色固体 |
| B、硫在氧气中燃烧,发出淡蓝色火焰,生成刺激性气味的气体 |
| C、碳在氧气中燃烧,发出白光,生成无色无味的气体 |
| D、磷在氧气中燃烧,生成白色的五氧化二磷 |
下列物质在氧气中燃烧,能产生白色固体的是( )
| A、铁丝 | B、红磷 | C、木炭 | D、硫粉 |
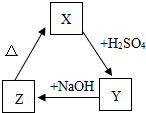 X、Y、Z之间存在如图转化关系:
X、Y、Z之间存在如图转化关系: