题目内容
氢氧化锂LiOH和NaOH的化学性质相似.“神舟”飞船内,可用盛有LiOH的过滤网吸收航天员呼出的气体,以降低CO2含量.则:
(1)请计算:用LiOH完全吸收176g CO2生成碳酸锂(化学式为Li2CO3)和水,理论上至少需要LiOH的质量是多少?
(2)请通过计算回答:飞船里使用的过滤网内选用氢氧化锂,而不用价格更便宜的氢氧化钠,其主要原因是 .
(1)请计算:用LiOH完全吸收176g CO2生成碳酸锂(化学式为Li2CO3)和水,理论上至少需要LiOH的质量是多少?
(2)请通过计算回答:飞船里使用的过滤网内选用氢氧化锂,而不用价格更便宜的氢氧化钠,其主要原因是
考点:根据化学反应方程式的计算,碱的化学性质
专题:有关化学方程式的计算,常见的碱 碱的通性
分析:(1)根据该反应的化学方程式可建立氢氧化锂和二氧化碳的质量关系,然后利用二氧化碳的质量可求出反应氢氧化锂的质量;
(2)根据二氧化碳的质量结合氢氧化钠和二氧化碳反应的化学方程式可以计算出176gCO2需要氢氧化钠的质量,然后进行比较即可.
(2)根据二氧化碳的质量结合氢氧化钠和二氧化碳反应的化学方程式可以计算出176gCO2需要氢氧化钠的质量,然后进行比较即可.
解答:解:(1)设需要氢氧化锂的质量为x
2LiOH+CO2═Li2CO3+H2O
48 44
x 176g
=
解得:x=192g
理论上至少需要LiOH的质量是192g
(2)设吸收176g CO2需要氢氧化钠的质量为y
CO2+2NaOH═Na2CO3+H2O
44 80
176g y
=
解得:y=320g
结合(1)的解答可以知道,吸收等质量的二氧化碳需要的氢氧化锂的质量要小,可以减轻火箭发射的重量.
故答案为:(1)192克;
(2)吸收相同质量的二氧化碳所需氢氧化锂的质量小,可以减轻火箭发射的重量.
2LiOH+CO2═Li2CO3+H2O
48 44
x 176g
| 48 |
| x |
| 44 |
| 176 |
解得:x=192g
理论上至少需要LiOH的质量是192g
(2)设吸收176g CO2需要氢氧化钠的质量为y
CO2+2NaOH═Na2CO3+H2O
44 80
176g y
| 44 |
| 176g |
| 80 |
| y |
解得:y=320g
结合(1)的解答可以知道,吸收等质量的二氧化碳需要的氢氧化锂的质量要小,可以减轻火箭发射的重量.
故答案为:(1)192克;
(2)吸收相同质量的二氧化碳所需氢氧化锂的质量小,可以减轻火箭发射的重量.
点评:本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
在加热KClO3制O2时,可作为催化剂的是( )
①二氧化锰 ②高锰酸钾 ③锰 ④锰酸钾.
①二氧化锰 ②高锰酸钾 ③锰 ④锰酸钾.
| A、① | B、①② |
| C、①②③ | D、①②③④ |
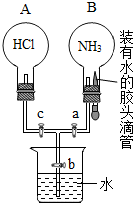

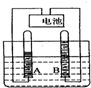 如图是电解水实验的示意图:
如图是电解水实验的示意图: