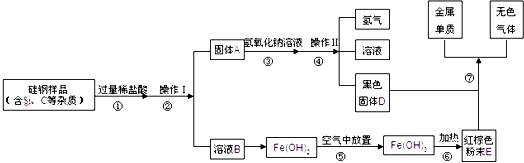
题目内容
某学生将带生锈的铁钉放入过量的稀盐酸中,他首先看到锈迹溶解,溶液呈 色,这是因为(用化学方程式表示) ;不一会儿,又看到溶液中有 的现象,这是因为铁钉部分溶解 (用化学方程式表示).
【考点】酸的化学性质;书写化学方程式、文字表达式、电离方程式.
【专题】常见的酸 酸的通性.
【分析】根据金属氧化物以及金属与酸的反应进行分析,铁锈的主要成分是氧化铁,能与盐酸反应生成氯化铁,其水溶液为黄色,铁能与盐酸反应生成氯化亚铁和氢气.
【解答】解:铁锈的主要成分是氧化铁,为红色,能与盐酸反应生成氯化铁,其水溶液为黄色,铁能与盐酸反应生成氯化亚铁和氢气,
故答案为:黄;Fe2O3+6HCl═2FeCl3+3H2O;气泡冒出;Fe+2HCl═FeCl2+H2↑.
【点评】本题考查了铁锈以及铁与盐酸反应的实验现象和化学方程式的书写,完成此题,可以依据已有的知识进行,需要同学们在品是的学习中加强基础知识的储备,以便灵活应用.

练习册系列答案
相关题目




 氢氧化钠溶液反应(Si+2NaOH+H2O═Na2SiO2+2H2↑).
氢氧化钠溶液反应(Si+2NaOH+H2O═Na2SiO2+2H2↑).