题目内容
5.下列有关实验现象的描述正确的是( )| A. | 铁丝在氧气中燃烧时火星四射,有黑色四氧化三铁固体生成 | |
| B. | 铁钉与稀盐酸反应后溶液由无色变成了蓝色 | |
| C. | 硫在空气中燃烧发出微弱的淡蓝色火焰 | |
| D. | 红磷在空气中燃烧,冒大量的白雾 |
分析 A、根据铁丝在氧气中燃烧的现象进行分析判断.
B、根据铁钉与稀盐酸反应的现象进行分析判断.
C、根据硫在空气中燃烧的现象进行分析判断.
D、根据红磷在空气中燃烧的现象进行分析判断.
解答 解:A、铁丝在氧气中剧烈燃烧,火星四射,有黑色四氧化三铁固体生成是实验结论而不是实验现象,故选项说法错误.
B、铁钉与稀盐酸反应后生成氯化亚铁和氢气,溶液由无色变成了浅绿色,故选项说法错误.
C、硫在空气中燃烧,发出微弱的淡蓝色火焰,故选项说法正确.
D、红磷在空气中燃烧,产生大量的白烟,而不是白雾,故选项说法错误.
故选:C.
点评 本题难度不大,掌握常见物质燃烧的现象即可正确解答,在描述物质燃烧的现象时,需要注意光和火焰、烟和雾、实验结论和实验现象的区别.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
16.下列说法正确的是( )
| A. | 饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 | |
| B. | 相同溶质的饱和溶液一定比不饱和溶液要浓 | |
| C. | 溶液中存在固体溶质时,该溶液一定是饱和溶液 | |
| D. | 在一定温度下,将饱和溶液中的水蒸发一部分,剩余溶液一定还是饱和溶液 |
20.用分子的性质可以解释下列现象,其中错误的是( )
| A. | 汽油挥发--分子体积变大 | |
| B. | 酒香不怕巷子深--分子在不断运动 | |
| C. | 向篮球中打气--分子间有间隔 | |
| D. | 氧化汞分解成汞和氧气--化学变化中分子可分 |
17.下列性质属于物理性质的是( )
| A. | 沸点 | B. | 酸性 | C. | 可燃性 | D. | 毒性 |
14.生活中常见的下列现象,属于化学变化的是( )
| A. | 干冰升华 | B. | 木炭的吸附作用 | C. | 工业制氧气 | D. | 光合作用 |
15.为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出).
【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
②碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
③本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
①连接仪器,并检查装置气密性.
②取一定量氧化铜,准确称得其质量为2.40g.
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测量并记录相关数据I(见表).
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表).
【实验装置】
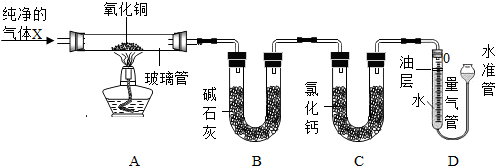
【相关数据】
【回答问题】
①B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
②实验过程中,当观察到量气管内液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的铜被氧化.
③分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
④通过计算推导出气体X的化学式为NH3;气体X还原氧化铜的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.
【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
②碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
③本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
①连接仪器,并检查装置气密性.
②取一定量氧化铜,准确称得其质量为2.40g.
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测量并记录相关数据I(见表).
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表).
【实验装置】

【相关数据】
| 数据编号 测量项目 | I | Ⅱ |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | 243.5 |
①B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
②实验过程中,当观察到量气管内液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的铜被氧化.
③分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
④通过计算推导出气体X的化学式为NH3;气体X还原氧化铜的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.

