题目内容
现取石灰石样品12g,加入50g稀盐酸恰好完全反应(假设杂质不溶于水且不与酸反应),最后称得剩余物的总质量为57.6g.计算:
(1)放出二氧化碳多少g?
(2) 石灰石中碳酸钙的质量分数.
(1)放出二氧化碳多少g?
(2) 石灰石中碳酸钙的质量分数.
分析:(1)根据质量守恒定律,放出二氧化碳的质量=反应前物质质量总和-反应后物质质量总和;
(2)利用碳酸钙与盐酸反应的化学方程式和生成二氧化碳的质量,列出比例式,就可计算出石灰石中碳酸钙的质量,然后根据质量分数公式计算即可.
(2)利用碳酸钙与盐酸反应的化学方程式和生成二氧化碳的质量,列出比例式,就可计算出石灰石中碳酸钙的质量,然后根据质量分数公式计算即可.
解答:解:(1)根据质量守恒定律,放出二氧化碳的质量=12g+50g-57.6g=4.4g;
(2)设参与反应的碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
∴
=
,
解之得:x=10g;
石灰石中碳酸钙的质量分数为:
×100%≈83.3%.
答:(1)放出二氧化碳4.4g;
(2)石灰石中碳酸钙的质量分数为83.3%.
(2)设参与反应的碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
∴
| 100 |
| 44 |
| x |
| 4.4g |
解之得:x=10g;
石灰石中碳酸钙的质量分数为:
| 10g |
| 12g |
答:(1)放出二氧化碳4.4g;
(2)石灰石中碳酸钙的质量分数为83.3%.
点评:本题主要考查学生利用化学方程式和质量守恒定律解答问题的能力.利用质量守恒定律,可以求出化学反应中生成气体和沉淀的质量,为进一步解题打开突破口.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
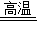 CaO+CO2↑.为了分析某石灰石的纯度,现取石灰石样品12g(设所含杂质不参加反应),充分煅烧后发现剩余固体质量为7.6g.求:
CaO+CO2↑.为了分析某石灰石的纯度,现取石灰石样品12g(设所含杂质不参加反应),充分煅烧后发现剩余固体质量为7.6g.求: