题目内容
用棉花团包住少量过氧化钠(淡黄色粉末,化学式Na2O2),在向其中通入一会儿二氧化碳气体后,棉花团便会燃烧起来.反应方程式为:2Na2O2+2CO2=2Na2CO3+O2;
(1)试分析棉花燃烧的原因;
(2)若有一火灾,用液态二氧化碳灭火器使其达到灭火.请说明灭火原理.
(1)试分析棉花燃烧的原因;
(2)若有一火灾,用液态二氧化碳灭火器使其达到灭火.请说明灭火原理.
考点:燃烧与燃烧的条件,灭火的原理和方法
专题:化学与生活
分析:根据已有的燃烧的条件进行分析解答,燃烧需要可燃物、可燃物与氧气接触且温度达到可燃物的着火点,灭火就是破坏燃烧的条件,据此解答.
解答:解:(1)棉花本身是可燃物,过氧化氢与二氧化碳反应生成氧气,且放出热量,温度达到棉花的着火点,则棉花能燃烧起来,故答案为:过氧化钠与二氧化碳反应生成氧气且放出的热量达到棉花的着火点;
(2)液态二氧化碳灭火器灭火是因为二氧化碳气化吸收热量能降低温度且二氧化碳能使可燃物与氧气隔绝,故答案为:降温的同时使可燃物与氧气隔绝.
(2)液态二氧化碳灭火器灭火是因为二氧化碳气化吸收热量能降低温度且二氧化碳能使可燃物与氧气隔绝,故答案为:降温的同时使可燃物与氧气隔绝.
点评:掌握燃烧的条件和灭火的原理是正确解答本题的关键.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、铝是地壳中含量最多的元素 |
| B、武德合金是制造保险丝的材料 |
| C、铜的化学性质不活泼,在潮湿的空气中不会被腐蚀 |
| D、锌的化学性质比铁活泼,铁的表面镀锌不能防止铁生锈 |

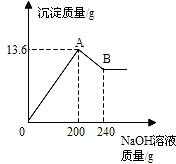 把MgCl2、AlCl3两种固体组成的混合物溶于水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量与生成沉淀质量如图所示.[已知:Al(OH)3+NaOH═NaAlO2+XH2O,NaAlO2可溶于水]) 试回答:
把MgCl2、AlCl3两种固体组成的混合物溶于水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量与生成沉淀质量如图所示.[已知:Al(OH)3+NaOH═NaAlO2+XH2O,NaAlO2可溶于水]) 试回答: