题目内容
20.下列是我们已学过的一些重要实验,请回答: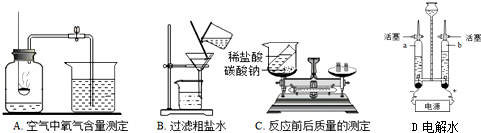
(1)A中红磷必须足量的原因是保证能完全地消耗瓶内空气中的氧气;
(2)B中玻璃棒的作用是引流;过滤后发现滤液仍然浑浊,可能的原因是滤纸破损或液面高于滤渣边缘(答出一点即可).
(3)C中反应后天平不平衡,该反应是否遵守质量守恒定律是(填“是”或“否”)
(4)D中发生反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑;a、b玻璃管中生成的气体质量比为1;8.
分析 (1)根据实验的原理及注意的事项分析红磷足量原因;
(2)根据玻璃棒在过滤操作的作用及实验操作分析浑浊的原因来分析;
(3)根据质量守恒定律的适用范围来分析;
(4)电解水生成氢气和氧气,结合方程式进行计算.
解答 解:(1)该实验主要是利用物质燃烧消耗装置内的氧气,然后根据进入水的体积,判断氧气的体积.只有加入过量的红磷,才能将将氧气完全消耗掉.如果红磷的量不足,会导致实验的结果是水倒流不足五分之一;故填:保证能完全地消耗瓶内空气中的氧气;
(2)在过滤操作中,玻璃棒的作用是引流;若滤纸破损或液面高于滤纸边缘,都会使滤液浑浊;故填:引流;滤纸破损或液面高于滤渣边缘;
(3)盐酸和碳酸钠反应产生二氧化碳气体跑到空气中去了,因此天平不平衡,但也正说明了符合质量守恒定律;故填:是;
(4)因为电解水能生成氢气和氧气,反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑,a管产生的是氢气,b管产生的是氧气,因此氢气和氧气的质量比为4:32=1:8;故填:2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑;1:8.
点评 此题以图示的形式综合考查了正确判断实验现象及规范进行基本的实验操作的综合题,解题时应充分利用题中给予的信息,进行筛选分析,得出正确答案.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.已知X元素的化合价为+2价,跟氧元素形成的化合物中,X元素的质量分数为60%,则X元素与氧元素组成的化合物的式量是( )
| A. | 24 | B. | 56 | C. | 40 | D. | 60 |
8.化学兴趣小组的同学对实验室中的一瓶冰状固体无水乙酸产生浓厚的兴趣,决定对这种酸与碱发生的反应展开探究.

资料摘要:
Ⅰ.无水乙酸(化学式可简写为HAc,Ac表示乙酸根)是一种有机酸,熔点16.6℃,在室温低于其熔点时,就会凝结成像冰一样的固体.
Ⅱ.无水硫酸铜是一种白色粉末,吸收水分后变成蓝色晶体.
【探究活动一】
乙酸溶液与氢氧化钠溶液混合后溶液酸碱性和溶质的变化
取一定量的无水乙酸配成溶液.向盛有10mL氢氧化钠溶液的烧杯中,逐滴加入乙酸溶液,搅拌使溶液均一,所加乙酸溶液的体积从V1到V7,依次增大,用pH计(用来精确测定溶液pH的仪器)依次测定烧杯中溶液的pH,所得数据如下:
(1)表中X值大于(选填“小于”、“等于”或“大于”)12.7.
(2)当加入乙酸溶液的体积为V5mL时,溶液呈中性.
(3)当烧杯中溶液的pH=6.5时,溶液中的溶质有NaAc和HAc(写化学式).
(4)乙酸溶液和氢氧化钠溶液混合没有明显现象,由上表分析,酸碱之间确实发生了化学反应的依据是烧杯中溶液的pH从大于7变为小于7.
【探究活动二】
无水乙酸与氢氧化钙反应有水生成兴趣小组同学将无水乙酸熔化后,进行如图11所示的实验.往三个广口瓶中分别加入试剂后,均迅速塞紧瓶塞,并使瓶内的试剂充分混合.
(5)往广口瓶中加入试剂后,迅速塞紧瓶塞,目的是防止空气中的水分进入广口瓶中,对实验造成干扰.
(6)观察到①和②两瓶中的白色无水硫酸铜均不变色,证明无水乙酸、氢氧化钙固体中均不含水.
(7)能证明无水乙酸与氢氧化钙反应有水生成的现象是无色硫酸铜变蓝.
【探究活动三】
(8)“探究活动一”和“探究活动二”用不同的实验方法证明了乙酸与碱确实能发生化学反应,请你另外设计一个实验方案再验证之:往滴有酚酞试液的氢氧化钠溶液逐滴滴入乙酸溶液,溶液由红色逐渐变成无色等合理
答案.

资料摘要:
Ⅰ.无水乙酸(化学式可简写为HAc,Ac表示乙酸根)是一种有机酸,熔点16.6℃,在室温低于其熔点时,就会凝结成像冰一样的固体.
Ⅱ.无水硫酸铜是一种白色粉末,吸收水分后变成蓝色晶体.
【探究活动一】
乙酸溶液与氢氧化钠溶液混合后溶液酸碱性和溶质的变化
取一定量的无水乙酸配成溶液.向盛有10mL氢氧化钠溶液的烧杯中,逐滴加入乙酸溶液,搅拌使溶液均一,所加乙酸溶液的体积从V1到V7,依次增大,用pH计(用来精确测定溶液pH的仪器)依次测定烧杯中溶液的pH,所得数据如下:
| 加入乙酸溶液的体积/mL | 0 | V1 | V2 | V3 | V4 | V5 | V6 | V7 |
| 烧杯中溶液的pH | X | 12.7 | 12.5 | 12.2 | 11.9 | 7.0 | 6.5 | 5.3 |
(2)当加入乙酸溶液的体积为V5mL时,溶液呈中性.
(3)当烧杯中溶液的pH=6.5时,溶液中的溶质有NaAc和HAc(写化学式).
(4)乙酸溶液和氢氧化钠溶液混合没有明显现象,由上表分析,酸碱之间确实发生了化学反应的依据是烧杯中溶液的pH从大于7变为小于7.
【探究活动二】
无水乙酸与氢氧化钙反应有水生成兴趣小组同学将无水乙酸熔化后,进行如图11所示的实验.往三个广口瓶中分别加入试剂后,均迅速塞紧瓶塞,并使瓶内的试剂充分混合.
(5)往广口瓶中加入试剂后,迅速塞紧瓶塞,目的是防止空气中的水分进入广口瓶中,对实验造成干扰.
(6)观察到①和②两瓶中的白色无水硫酸铜均不变色,证明无水乙酸、氢氧化钙固体中均不含水.
(7)能证明无水乙酸与氢氧化钙反应有水生成的现象是无色硫酸铜变蓝.
【探究活动三】
(8)“探究活动一”和“探究活动二”用不同的实验方法证明了乙酸与碱确实能发生化学反应,请你另外设计一个实验方案再验证之:往滴有酚酞试液的氢氧化钠溶液逐滴滴入乙酸溶液,溶液由红色逐渐变成无色等合理
答案.
15.在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
通过分析,判断下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 3 | 5 | 20 | 7 |
| 反应后质量/g | 10 | 5 | 8 | m |
| A. | m为12g | B. | 该反应是化合反应 | ||
| C. | 乙物质一定是催化剂 | D. | 反应中甲、丙的质量比为10:8 |
9.化学与日常生活有着密切联系.下列说法错误的是( )
| A. | 人体缺铁会引起贫血,因此应补充铁粉 | |
| B. | 垃圾分类回收既可以充分利用资源又可以减少环境污染 | |
| C. | 肥皂水区分硬水和软水时,泡沫少的是硬水,泡沫多的是软水 | |
| D. | 发生火灾时,要视不同的可燃物选择不同的灭火方法和灭火剂 |
14.比较化学学习中常用的思维方法.下列相关知识的比较中,关系正确的是( )
| A. | 同压下凝固点:蒸馏水<氯化钠溶液 | B. | 着火点:纸片>煤炭 | ||
| C. | 含碳量:甲醛(CH2O)=醋酸(C2H4O2) | D. | 相对分子质量:油脂>甲烷 |