题目内容
10.已知X元素的化合价为+2价,跟氧元素形成的化合物中,X元素的质量分数为60%,则X元素与氧元素组成的化合物的式量是( )| A. | 24 | B. | 56 | C. | 40 | D. | 60 |
分析 利用化合价确定化合物中X元素与氧元素的原子个数关系,然后由氧元素的质量分数得出化合物中X元素与氧元素的质量比,最后运用元素质量比、相对原子质量及原子个数关系求出X元素的相对原子质量.
解答 解:根据化合物中各元素化合价代数和为0,某+2价的X元素与氧元素(-2价)形成的化合物中,X元素与氧元素的原子个数比为1:1;
化合中X元素的质量分数为60%,则X元素与氧元素质量比=60%:(1-60%)=3:2;
设此X元素的相对原子质量为x,则X元素与氧元素质量比为:(x×1):(16×1)=3:2;则x=24;
因此,X元素的相对原子质量为24.
故选:A.
点评 元素质量比、相对原子质量及原子个数间的关系为:元素质量比等于元素的相对原子质量与原子个数乘积之比.

练习册系列答案
相关题目
20.只含铜和氧两种元素的固体样品9.0g,测得铜的质量为8.0g,已知铜的氧化物有CuO和Cu2O,下列说法错误的是( )
| A. | 固体样品可能由三种物质组成 | B. | 固体样品是CuO与Cu2O的混合物 | ||
| C. | 固体样品可能是Cu2O | D. | 固体样品可能由CuO和Cu组成 |
1.下列物质在氧气中燃烧,其中可观察到明亮的蓝紫色火焰现象的是( )
| A. |  木炭 | B. |  红磷 | C. |  铁丝 | D. |  硫粉 |
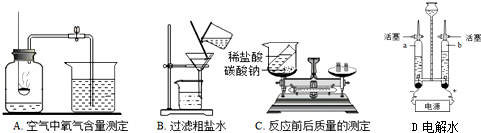
2.规范的实验操作是科学探究的基础.下列图示实验操作正确的是( )
| A. | 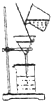 过滤 | B. |  二氧化碳验满 | C. | 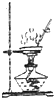 蒸发 | D. | 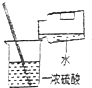 稀释浓硫酸 |
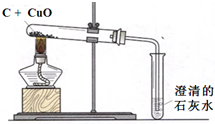 如图为木炭还原氧化铜的实验装置(石灰水足量).某同学为了探究木炭还原氧化铜后的气体产物是什么?
如图为木炭还原氧化铜的实验装置(石灰水足量).某同学为了探究木炭还原氧化铜后的气体产物是什么?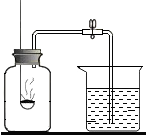 同学用如图所示的装置来测定空气中氧气的含量.
同学用如图所示的装置来测定空气中氧气的含量.