题目内容
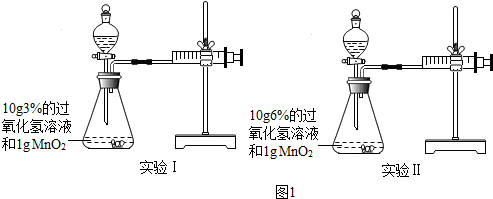
实验室里有四只编号为Ⅰ、Ⅱ、Ⅲ、Ⅳ但无试剂名称标签的试剂瓶,分别盛有盐酸、氯化镁溶液、氢氧化钠溶液和硫酸钠溶液.为确认试剂名称,进行如下三个实验(还可使用硝酸银溶液),实验均没有明显现象.
(a)向溶液Ⅰ中滴入少量溶液Ⅱ,在所得的混和溶液中滴加少量的溶液Ⅲ;
(b)将溶液Ⅰ加入溶液Ⅲ中;
(c)向溶液Ⅳ中滴加少量硝酸银溶液(溶液较稀,微溶物不产生沉淀).
请回答下列问题.
(1)盐酸是 号,硫酸钠是 号.
(2)先将Ⅱ与Ⅲ混和,再加入I现象是 ,有关的化学方程式是 .
(a)向溶液Ⅰ中滴入少量溶液Ⅱ,在所得的混和溶液中滴加少量的溶液Ⅲ;
(b)将溶液Ⅰ加入溶液Ⅲ中;
(c)向溶液Ⅳ中滴加少量硝酸银溶液(溶液较稀,微溶物不产生沉淀).
请回答下列问题.
(1)盐酸是
(2)先将Ⅱ与Ⅲ混和,再加入I现象是
考点:酸、碱、盐的鉴别,书写化学方程式、文字表达式、电离方程式
专题:物质的鉴别题
分析:四种物质中,IV加入硝酸银后没有沉淀,说明IV是硫酸钠;盐酸和氯化镁不反应,和氢氧化镁反应都没有现象,所以溶液Ⅰ是盐酸,溶液Ⅱ和Ⅲ是氯化镁溶液、氢氧化钠溶液中的一种,两个无法确定.
解答:解:(1)四种物质中,IV加入硝酸银后没有沉淀,说明IV是硫酸钠;盐酸和氯化镁不反应,和氢氧化镁反应都没有现象,所以溶液Ⅰ是盐酸,溶液Ⅱ和Ⅲ是氯化镁溶液、氢氧化钠溶液中的一种,两个无法确定.
(2)氯化镁溶液和氢氧化钠溶液反应生成氢氧化镁沉淀,加入稀盐酸后,氢氧化镁与盐酸生成氯化镁和水,沉淀溶解.反应方程式为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl;Mg(OH)2+2HCl=MgCl2+2H2O.
故答案为:(1)I;IV;
(2)先出现白色沉淀,然后白色沉淀溶解;2NaOH+MgCl2=Mg(OH)2↓+2NaCl;Mg(OH)2+2HCl=MgCl2+2H2O
(2)氯化镁溶液和氢氧化钠溶液反应生成氢氧化镁沉淀,加入稀盐酸后,氢氧化镁与盐酸生成氯化镁和水,沉淀溶解.反应方程式为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl;Mg(OH)2+2HCl=MgCl2+2H2O.
故答案为:(1)I;IV;
(2)先出现白色沉淀,然后白色沉淀溶解;2NaOH+MgCl2=Mg(OH)2↓+2NaCl;Mg(OH)2+2HCl=MgCl2+2H2O
点评:本题考查了复分解反应,完成此题,可以依据物质的性质进行.要求同学们加强对物质性质以及物质间反应的实验现象的掌握,以便灵活应用.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
下列化学方程式符合实际,且属于置换反应的是( )
| A、FeCl3+NaOH═Fe(OH)3↓+3NaCl | ||||
B、CO+CuO
| ||||
C、C+2CuO
| ||||
| D、NaOH+HCl═NaCl+H2O |
下列关于“物质-用途-性质”的说法不正确的是( )
| A、氧气--火箭发射--可燃性 |
| B、炭黑--制油墨--通常状况下性质稳定 |
| C、氮气--食品防腐--常温下化学性质稳定 |
| D、稀有气体--霓虹灯--通电能发出不同颜色的光 |
学习化学的目的是运用化学知识解释日常生活中的现象,分析和解决生产生活中的实际问题.下列说法中你认为错误的是( )
| A、搅拌能加快蔗糖在水中的溶解,其原因是增大了蔗糖的溶解度 |
| B、油库、面粉厂、纺织厂、煤矿矿井内都要严禁烟火 |
| C、去除油污时洗涤剂起到的是乳化作用 |
| D、敞口放置的酒精没有燃烧的原因是温度没有达到酒精的着火点 |