题目内容
二甲醚(C2H6O)作为一种新能源,有关说法正确的是( )
|
| A. | 二甲醚的相对分子质量为48 |
|
| B. | 二甲醚属于氧化物 |
|
| C. | 二甲醚由2个碳原子、6个氢原子和1个氧原子构成 |
|
| D. | 二甲醚中碳元素与氢元素的质量比为4:1 |
| 相对分子质量的概念及其计算;从组成上识别氧化物;原子的有关数量计算;元素质量比的计算.. | |
| 专题: | 化学式的计算. |
| 分析: | A、根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答;B、根据氧化物是指由两种元素组成且其中一种是氧元素的化合物,进行判断; C、根据标在元素符号右下角的数字表示一个分子中所含原子的个数;进行解答;D、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答. |
| 解答: | 解:A、根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得二甲醚的相对分子质量为 12×2+6+16=46;故A说法错误; B、根据氧化物是指由两种元素组成且其中一种是氧元素的化合物,判断二甲醚不属于氧化物;故B说法错误; C、根据标在元素符号右下角的数字表示一个分子中所含原子的个数;每个二甲醚分子由2个碳原子、6个氢原子和1个氧原子构成;故C说法错误; D、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得二甲醚中碳元素与氢元素的质量比为 (12×2):6=4:1,故D说法正确; 故选D. |
| 点评: | 解答此类题必须区分清:化合物中各元素质量比与原子个数比,才能顺利解答. |

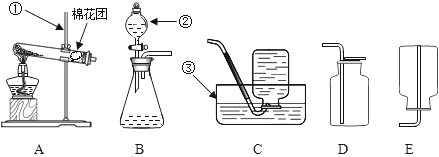
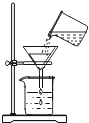
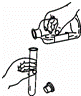
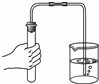
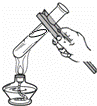
如图所示实验操作正确的是( )
|
| A. |
过滤 | B. |
倾倒液体 | C. |
检查气密性 | D. |
加热液体 |
在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
| 物质 | W | G | H | P |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | 待测 | 26 | 2 | 12 |
对该反应的认识正确的是( )
|
| A. | W待测值是13 | B. | 该反应是分解反应 |
|
| C. | P是生成物 | D. | 物质H是该反应的催化剂 |
若阴离子X2﹣含有10个电子,下列不能确定的是( )
|
| A. | 元素原子中的质子数 | B. | 元素种类 |
|
| C. | 粒子X2﹣所含中子数 | D. | 此粒子与Mg2+结合时离子个数比 |
在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。
 |
请回答以下问题:
(1)A中氮元素和氢元素的质量比为_____ ;
(2)该反应的化学方程式 ________ ; 
(3)该反应的基本反应类型为_____。