题目内容
在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
| 物质 | W | G | H | P |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | 待测 | 26 | 2 | 12 |
对该反应的认识正确的是( )
|
| A. | W待测值是13 | B. | 该反应是分解反应 |
|
| C. | P是生成物 | D. | 物质H是该反应的催化剂 |
| 质量守恒定律及其应用.. | |
| 专题: | 化学用语和质量守恒定律. |
| 分析: | 根据质量守恒定律可知,参加反应的各物质质量总和等于反应后生成的各物质的质量总和.化学反应后,质量增加的物质是生成物,质量减少的物质是反应物.利用这一性质进行判断. |
| 解答: | 解:由表中信息可知,P物质的质量减少为反应物,参加反应的质量是20克;G物质的质量增加为生成物,生成的质量是25克;H物质的质量不变故H物质不参与反应.根据质量守恒定律可知,W是反应物,参加反应的质量是5克. A、反应后物质W的质量为:18g﹣5g=13g.故A正确; B、反应物是两种,生成物是一种,属于化合反应,故B错误; C、P物质的质量减少故为反应物.故C错误; D、物质H的质量在反应前后不变,可能是该反应的催化剂,故D错误. 故选A. |
| 点评: | 在化学反应中遵循质量守恒定律,参加反应的物质的质量等于反应后生成的物质的质量. |

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案下列取用试剂的操作图示错误的是( )
|
| A. |
用药匙取用粉末 | B. |
用纸槽取用粉末 | C. |
倾倒液体 | D. |
取用块状固体 |
二甲醚(C2H6O)作为一种新能源,有关说法正确的是( )
|
| A. | 二甲醚的相对分子质量为48 |
|
| B. | 二甲醚属于氧化物 |
|
| C. | 二甲醚由2个碳原子、6个氢原子和1个氧原子构成 |
|
| D. | 二甲醚中碳元素与氢元素的质量比为4:1 |
已知A、B为两种黑色粉末,D为红色单质。A、B、C、D、E五种物质之间的转化关系如图10所示。
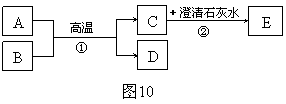 |
请回答:
(1)C的化学式为 ________ ;
(2)A中金属元素的化合价是______ __;
__;
(3)反应①的化学方程式为 ________;
该反应的基本类型是 _____ ___。
___。