题目内容
4. 三位同学用如图所示装置做一氧化碳还原氧化铁的实验.当观察到玻璃管A中的粉末由红棕色逐渐变为黑色时,停止加热,继续通一氧化碳,冷却到室温,停止通气,同时观察到澄清的石灰水变浑浊.
三位同学用如图所示装置做一氧化碳还原氧化铁的实验.当观察到玻璃管A中的粉末由红棕色逐渐变为黑色时,停止加热,继续通一氧化碳,冷却到室温,停止通气,同时观察到澄清的石灰水变浑浊.用一氧化碳还原氧化铁的实验装置
小明认为:依据上述实验现象可以判断出生成的黑色固体为金属铁.
小红认为:仅从上述实验现象,不足以证明生成的黑色固体为金属铁,她增加了一个实验:用磁铁靠近生成的黑色固体,看到有黑色固体被磁铁吸引.于是得出生成的黑色固体为金属铁的结论.
小光通过查询有关资料得知:
(1)一氧化碳与氧化铁在加热条件下,可发生如下反应:
3Fe2O3+CO$\frac{\underline{\;\;△\;\;}}{\;}$2Fe3O4+CO2
(2)四氧化三铁(Fe3O4)为黑色固体,有强磁性,能够被磁铁吸引.因此,小光认为小明和小红的结论都不能成立,你是否同意他的说法?同意.请具体说明你的理由:根据资料可知,生成的Fe3O4也是黑色固体且能被磁铁吸引,同时生成的CO2也能使澄清石灰水变浑浊.
小光欲通过实验检验生成的黑色固体是否含有金属铁.请你帮他设计实验并填写下表.
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
取少量黑色固体于试管中,向其中滴加稀盐酸 | 若产生气泡 若没有气泡产生 | 则黑色固体中含金属铁 则黑色固体中不含金属铁 |
分析 由题意可知:“四氧化三铁为黑色固体,有强磁性,能够被磁铁吸引”,所以只根据此现象,不能确定生成物;并根据铁能与稀硫酸反应产生气泡进一步实验验证.
解答 解:由题意“生成黑色固体”,而资料中的:一氧化碳与氧化铁在加热条件下可能会生成四氧化三铁,且四氧化三铁也是黑色的固体,有强磁性,能够被磁铁吸引;所以只根据此现象:有黑色固体被磁铁吸引,不能确定生成物;故小光认为小明和小红的结论都不能成立,具体理由为:根据资料可知:一氧化碳与氧化铁在加热条件下可能会生成四氧化三铁,Fe3O4也是黑色固体且能被磁铁吸引;
铁与稀硫酸反应可产生气体---氢气,所以,可取少量黑色固体于试管中,向其中滴加稀硫酸,观察是否有气泡产生;如果有气泡产生,则黑色固体为铁;若没有气泡产生,则黑色固体中不含金属铁.
故答案为:同意;根据资料可知,生成的Fe3O4也是黑色固体且能被磁铁吸引,同时生成的CO2也能使澄清石灰水变浑浊;
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 取少量黑色固体于试管中,向其中滴加稀盐酸 | 若产生气泡 若没有气泡产生 | 则黑色固体中含金属铁 则黑色固体中不含金属铁 |
点评 掌握铁的化学性质:与酸反应生成气体,结合现象推测结论(反应本质).

练习册系列答案
相关题目
3.根据表提供的信息,下列判断正确的是( )
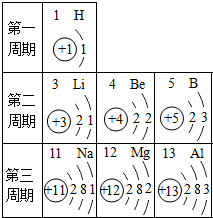

| A. | 元素所在的周期数等于其原子的电子层数 | |
| B. | 钠离子核外有三个电子层 | |
| C. | 在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+2 | |
| D. | 第二、三周期元素的原子从左至右最外层电子数逐渐增多 |
12.下列变化属于化学变化的是( )
| A. | 活性炭吸附 | B. | 铁钉生锈 | C. | 灯泡通电发光 | D. | 氧气液化 |
19.现有25g久置的生石灰,测得其中钙元素与碳元素的质量比为10:1,在室温下,将该化合物与100g稀盐酸混合,恰好完全反应,所得的不饱和溶液的质量为120.6g,则原化混合物中钙元素的质量为( )
| A. | 10g | B. | 12g | C. | 14g | D. | 16g |
9.下列转化必需通过化学变化才能实现的是( )
| A. | 由化合物变为单质 | |
| B. | 由混合物变为纯净物 | |
| C. | 由固态变为气态 | |
| D. | 由一种分子构成的物质变为多种分子构成的物质 |
13.将下列物质同时加到水中,能大量共存且得到无色透明溶液的是( )
| A. | KOH、HCl、( NH4)2 SO4 | B. | K2CO3、Ba (NO3)2、NaOH | ||
| C. | FeCl3、NaCl、KNO3 | D. | CaCl2、HCl、NaNO3 |


