题目内容
4.敞口放置的氢氧化钠容易吸水和变质.实验室中有150g久置的氢氧化钠固体样品(假设样品中各成分的分布是均匀的).某实验小组从该样品中取出20g,加热烘干其中的水分,得到18.4g固体.向所得固体中加入过量的澄清石灰水,充分反应后得到10g沉淀.试计算未变质前的氢氧化钠质量.分析 根据氢氧化钠与碳酸钠的性质,氢氧化钠与澄清石灰水不反应,碳酸钠与石灰水生成碳酸钙沉淀和氢氧化钠,根据反应的化学方程式和物质的均一性由生成碳酸钙沉淀的质量计算出样品中的碳酸钠和变质的氢氧化钠的质量;然后求出未变质前的氢氧化钠质量.
解答 解:因为 20g 样品烘干后得到18.6g 固体,加入石灰水后得到10g沉淀;所以剩余150g样品中含有的碳酸钠和氢氧化钠固体共有$\frac{150g}{20g}$×18.4g=138g 固体,加入澄清石灰水后得到碳酸钙有$\frac{150g}{20g}$×10g=75g.
由CO2+2NaOH=Na2CO3+H2O;Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
可得变质的氢氧化钠的质量与碳酸钙之间的质量为:
2NaOH~CaCO3↓
设变质的氢氧化钠的质量x,碳酸钠的质量为y,
2NaOH~Na2CO3~CaCO3↓
80 106 100
x y 75g
$\frac{80}{x}$=$\frac{100}{75g}$
x=60g
$\frac{106}{y}$=$\frac{100}{75g}$
y=79.5g
所得没有变质的氢氧化钠的质量为138g-79.5g=58.5g
未变质前的氢氧化钠质量58.5g+60g=118.5g
答:未变质前的氢氧化钠质量为118.5g.
点评 根据反应的化学方程式可以表示反应中各物质的质量关系,由反应中某物质的质量可计算反应中其它物质的质量.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案
相关题目
15.下列图①~④分别与相应的操作过程相对应,其中正确的是( )
| A. | 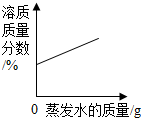 在恒温的条件下,将足量的氯化钠饱和溶液蒸发适量的水分 | |
| B. |  向露置在空气中部分变质的氢氧化钠溶液中加入稀盐酸 | |
| C. |  向氢氧化钠溶液中不断加水稀释 | |
| D. |  相同质量的且过量的锌粉和铁粉,分别与质量和质量分数相同的稀盐酸反应 |
16.葡萄酒中含有单宁,它十分有益于心血管疾病的预防.单宁的化学式是C76H52O46.下列有关单宁的说法不正确的是( )
| A. | 单宁属于有机物 | B. | 单宁中碳、氢元素的质量比为19:13 | ||
| C. | 每个单宁分子中含有174个原子 | D. | 单宁中氧元素的质量分数最高 |
14. 悉尼科技大学的研究小组研发了一种独特的复合材料--石墨纸,如图所示.其成分以石墨为主,薄如纸张,比钢要坚硬10倍且轻巧,还可以回收再利用,未来应用非常广泛.下列说法错误的是( )
悉尼科技大学的研究小组研发了一种独特的复合材料--石墨纸,如图所示.其成分以石墨为主,薄如纸张,比钢要坚硬10倍且轻巧,还可以回收再利用,未来应用非常广泛.下列说法错误的是( )
 悉尼科技大学的研究小组研发了一种独特的复合材料--石墨纸,如图所示.其成分以石墨为主,薄如纸张,比钢要坚硬10倍且轻巧,还可以回收再利用,未来应用非常广泛.下列说法错误的是( )
悉尼科技大学的研究小组研发了一种独特的复合材料--石墨纸,如图所示.其成分以石墨为主,薄如纸张,比钢要坚硬10倍且轻巧,还可以回收再利用,未来应用非常广泛.下列说法错误的是( )| A. | 与同体积的钢相比,石墨纸的质量较小 | |
| B. | 与钢相比,石墨纸的硬度较大 | |
| C. | 石墨纸是一种环保材料 | |
| D. | 石墨纸是绝缘体,不易导电 |
 用符号表示:
用符号表示: