题目内容
20.汽车尾气排气管使用催化剂,可使有毒气体转变为无毒气体(徽观示意图中,“ ”表示碳原子、“
”表示碳原子、“ ”表示氮原子、“
”表示氮原子、“ ”表示氧原子).下列说法错误的是( )
”表示氧原子).下列说法错误的是( )
| A. | 反应前后碳元素的化合价发生了变化 | |
| B. | 反应后有三种物质生成 | |
| C. | 参加反应的两种分子的个数比为1:1 | |
| D. | 反应中有单质生成 |
分析 根据变化微观示意图及粒子构成模拟图,可判断该变化为两种化合物的分子通过原子的重新结合生成一种单质分子和一种化合物分子,要特别注意有一个分子没有参加反应.
解答 解:A、反应前后碳元素的化合价由+2价变成了+4价,发生了变化;故A说法正确;
B、由图示可知,反应后有两种物质生成;故B说法错误;
C、反应前后都有1个构成相同的化合物的分子,说明该分子未参加反应,因此,参加反应的两种分子的个数比为1:1;故说法正确;
D、生成物分子中有同种原子构成的单质分子,因此反应中有单质生成;故说法正确;
故选B.
点评 根据变化微观示意图及粒子构成模拟图,根据分子由原子构成等特点,正确判断变化中的物质构成与粒子个数关系,是解答本题的基本方法.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
10.实验室常用图1装置制取气体,请你根据所学知识回答下列问题.
(1)仪器a的名称是酒精灯,a应在固定试管之前(选填“前”或“后”)放置.
(2)实验室制取氧气时,常用A装置制取并在试管口塞一团棉花,其化学反应方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若选用B装置制取,其化学反应方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.选用的收集装置是C(填字母序号)若改用如图2装置收集气体,则气体应从b进(填“a”或“b”)
(3)甲同学在实验室制取二氧化碳的研究中,进行了如下实验:
Ⅰ.上述实验中反映的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O.
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号).
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积);.
Ⅳ.研究发现酸的浓度越大,产生的气体的速度越快,与甲比较,对丁分析正确的是AB
A.反应更为剧烈 B.最终剩余溶液的质量更小
C.产生的二氧化碳的质量更大 D.粉末状大理石利用率更高
(4)乙同学也取了一定浓度的盐酸与石灰石反应制取气体,并将生成的气体通入澄清石灰水中,未见变浑浊.为探究其原因,进行了如下过程:
【作出猜想】
A.石灰水已经完全变质; B.气体中有挥发出来的HCl气体.
【实验探究】
①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液变红色.于是排除了猜想A,你认为排除猜想A的理由是酚酞试液变红,说明溶液中存在碱性物质Ca(OH)2.
②乙同学想探究所得气体中是否有挥发出来的HCl气体,设计如下实验.请你帮他完成实验,填写以下表格:
【查阅资料】
碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O=2NaHCO3
【拓展延伸】
如果用上述原料制得纯净的二氧化碳气体,所选仪器的连接顺序为BHEC(填字母).
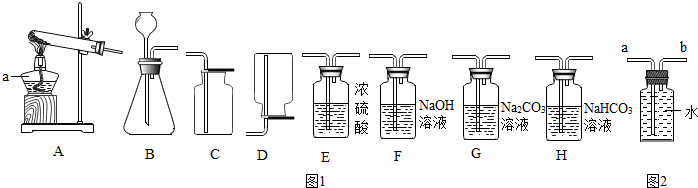
(1)仪器a的名称是酒精灯,a应在固定试管之前(选填“前”或“后”)放置.
(2)实验室制取氧气时,常用A装置制取并在试管口塞一团棉花,其化学反应方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若选用B装置制取,其化学反应方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.选用的收集装置是C(填字母序号)若改用如图2装置收集气体,则气体应从b进(填“a”或“b”)
(3)甲同学在实验室制取二氧化碳的研究中,进行了如下实验:
| 药品实验编号 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号).
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积);.
Ⅳ.研究发现酸的浓度越大,产生的气体的速度越快,与甲比较,对丁分析正确的是AB
A.反应更为剧烈 B.最终剩余溶液的质量更小
C.产生的二氧化碳的质量更大 D.粉末状大理石利用率更高
(4)乙同学也取了一定浓度的盐酸与石灰石反应制取气体,并将生成的气体通入澄清石灰水中,未见变浑浊.为探究其原因,进行了如下过程:
【作出猜想】
A.石灰水已经完全变质; B.气体中有挥发出来的HCl气体.
【实验探究】
①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液变红色.于是排除了猜想A,你认为排除猜想A的理由是酚酞试液变红,说明溶液中存在碱性物质Ca(OH)2.
②乙同学想探究所得气体中是否有挥发出来的HCl气体,设计如下实验.请你帮他完成实验,填写以下表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 将生成的气体通入AgNO3溶液中 | 产生白色沉淀 | 气体中有HCl |
碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O=2NaHCO3
【拓展延伸】
如果用上述原料制得纯净的二氧化碳气体,所选仪器的连接顺序为BHEC(填字母).

8.下列几种物品所使用的材料中属于无机材料的是( )


| A. | ①② | B. | ①③ | C. | ②③⑤ | D. | ②④ |
12.除去下列各组物质中杂质,所用试剂和方法均正确的是( )
| 选项 | 物质 | 杂质 | 除杂所用试剂和方法 |
| A | CaCl2溶液 | 稀HCl | 加入过量的碳酸钙,过滤 |
| B | NaOH溶液 | Ca(OH)2溶液 | 先加入过量Na2CO3溶液,再过滤 |
| C | CO2 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| D | CaO | CaCO3 | 加入适量的蒸馏水,过滤,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
9. 妈妈买来一袋加碘食盐,包装袋上的部分说明如图所示,小林取出部分加碘食盐带到实验室,与同学们一起进行实验探究.
妈妈买来一袋加碘食盐,包装袋上的部分说明如图所示,小林取出部分加碘食盐带到实验室,与同学们一起进行实验探究.
(1)食盐是比较稳定的,而说明中强调“防热”是否因为受热会造成碘的损失?
老师指导他们将一定浓度的碘酸钾溶液分成5等份,于不同温度下加热十分钟后,测定碘酸钾浓度,计算碘损失率并记录如下
分析上表可得出的结论是温度升高,碘损失率增大.
交流反思:烧菜时最好(填系好)B放加碘盐.
A.加菜后马上 B.菜出锅前
(2)烧菜时加醋对碘的损失率是否也有影响?请你和他们一起设计实验方案取两支试管分别加入相同浓度、相同质量(或体积)的碘酸钾溶液,向其中一支试管中加入少许食醋(或醋酸、稀盐酸等),然后将两支试管同时放入100℃水浴(相同温度)中加热十分钟(加热相同时间)后,测定测定碘酸钾浓度,计算碘损失率.
(3)为了排除实验过程中偶然因素干扰,保证实验结果的可靠性,你认为还应该如何完善你的实验方案?重复实验(多次测量求平均值等).
 妈妈买来一袋加碘食盐,包装袋上的部分说明如图所示,小林取出部分加碘食盐带到实验室,与同学们一起进行实验探究.
妈妈买来一袋加碘食盐,包装袋上的部分说明如图所示,小林取出部分加碘食盐带到实验室,与同学们一起进行实验探究.(1)食盐是比较稳定的,而说明中强调“防热”是否因为受热会造成碘的损失?
老师指导他们将一定浓度的碘酸钾溶液分成5等份,于不同温度下加热十分钟后,测定碘酸钾浓度,计算碘损失率并记录如下
| 温度 | 30℃水浴 | 50℃水浴 | 80℃水浴 | 100℃水浴 | 煮沸 |
| 碘损失率(%) | 0 | 0.3 | 0.67 | 1 | 5.56 |
交流反思:烧菜时最好(填系好)B放加碘盐.
A.加菜后马上 B.菜出锅前
(2)烧菜时加醋对碘的损失率是否也有影响?请你和他们一起设计实验方案取两支试管分别加入相同浓度、相同质量(或体积)的碘酸钾溶液,向其中一支试管中加入少许食醋(或醋酸、稀盐酸等),然后将两支试管同时放入100℃水浴(相同温度)中加热十分钟(加热相同时间)后,测定测定碘酸钾浓度,计算碘损失率.
(3)为了排除实验过程中偶然因素干扰,保证实验结果的可靠性,你认为还应该如何完善你的实验方案?重复实验(多次测量求平均值等).
10.下列事实和解释不相符的是( )
| A. | 汽油洗油污--汽油能溶解油污 | |
| B. | 熟石灰调节酸性土壤--熟石灰显碱性 | |
| C. | 活性炭净水--活性炭能吸附水中的一些杂质 | |
| D. | 石墨可做电极材料--石墨质软 |
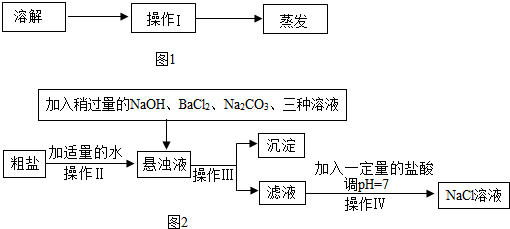
 有四种常见的酸、碱或盐的溶液,用如图所示的化学分析方法鉴别它们:
有四种常见的酸、碱或盐的溶液,用如图所示的化学分析方法鉴别它们: