题目内容
4.100g5%的KCl溶液中加入25g水中后,该溶液中溶质的质量分数4%,在20℃时,在加水后的溶液中再加25gKCl,此时KCl的质量分数20%,此时溶液是否达到饱和?否(20℃KCl溶解度为34g)分析 根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%,结合题意进行分析解答即可.
解答 解:100g5%的KCl溶液中加入25g水中后,该溶液中溶质的质量分数为$\frac{100g×5%}{100g+25g}$×100%=4%;
其中KCl为100g×5%=5g;水为100g+25g-5g=120g;
20℃KCl溶解度为34g,即20℃时100g水中最多溶解KCl为34g,120g水中最多溶解KCl为40.8g,所以在20℃时,在加水后的溶液中再加25gKCl,KCl质量为25g+5g=30g,所以此时溶液没有达到饱和;此时KCl的质量分数为$\frac{30g}{100g+25g+25g}$×100%=20%
故答案为:4%;20%;否.
点评 本题难度不大,掌握溶质质量分数的有关计算并能灵活运用即可正确解答本题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
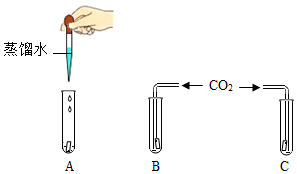 为证明CO2能与水反应,设计了如图所示的实验,图中A、B、C分别为用石蕊溶液染成的紫色干燥的滤纸,分析回答问题
为证明CO2能与水反应,设计了如图所示的实验,图中A、B、C分别为用石蕊溶液染成的紫色干燥的滤纸,分析回答问题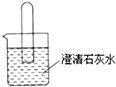 如图所示,将一个充满二氧化碳的试管倒立在盛有澄清石灰水的烧杯中,
如图所示,将一个充满二氧化碳的试管倒立在盛有澄清石灰水的烧杯中,